Augustus 20, 2018
High Flow Nasal Cannula (HFNC) – Deel 1: Hoe Het Werkt
 Het gebruik van verwarmde en bevochtigde high flow nasal cannula (HFNC) is steeds populairder geworden bij de behandeling van patiënten met acuut ademhalingsfalen in alle leeftijdsgroepen. Ik begon het te gebruiken als een pediatrische intensive care fellow, maar had weinig kennis over hoe het eigenlijk werkte. Een paar jaar nadat ik het met succes had gebruikt bij kinderen, vooral bij ernstige bronchiolitis, merkte ik dat we het ook begonnen te gebruiken op de intensive care-afdeling voor volwassenen. Het lijkt erop dat er de laatste jaren veel studies zijn verschenen over de werkingsmechanismen en het gebruik bij verschillende aandoeningen. In dit deel vatten we samen hoe het werkt en in deel 2 bespreken we de belangrijkste indicaties voor het gebruik ervan bij volwassen en pediatrische patiënten.
Het gebruik van verwarmde en bevochtigde high flow nasal cannula (HFNC) is steeds populairder geworden bij de behandeling van patiënten met acuut ademhalingsfalen in alle leeftijdsgroepen. Ik begon het te gebruiken als een pediatrische intensive care fellow, maar had weinig kennis over hoe het eigenlijk werkte. Een paar jaar nadat ik het met succes had gebruikt bij kinderen, vooral bij ernstige bronchiolitis, merkte ik dat we het ook begonnen te gebruiken op de intensive care-afdeling voor volwassenen. Het lijkt erop dat er de laatste jaren veel studies zijn verschenen over de werkingsmechanismen en het gebruik bij verschillende aandoeningen. In dit deel vatten we samen hoe het werkt en in deel 2 bespreken we de belangrijkste indicaties voor het gebruik ervan bij volwassen en pediatrische patiënten.
De verwarmde en bevochtigde hoge flow neuscanule of zoals de meesten het noemen, Hi Flow Nasal Cannula (HFNC), is niet zomaar een standaard neuscanule die wordt aangezwengeld tot een zeer hoog debiet. Het neemt eigenlijk gas en kan het aan 37 o C met een 100% relatieve vochtigheid verwarmen en kan 0.21 – 1.00% fi02 bij stroomtarieven van zelfs 60 liters/min. leveren. Het stroomtarief en fi02 kunnen onafhankelijk worden getitreerd gebaseerd op de stroom van uw patiënt en fi02 requirements.

Er zijn 2 hoofdbedrijven, die deze apparaten vervaardigen: Vapotherm die een apparaat heeft dat stroomsnelheden tot 50 liter/min kan leveren en Fisher Paykall die zowel de Optiflow als de AIRVO 2 apparaten biedt die beide stroomsnelheden tot 60 liter/min kunnen leveren.
 Elk bedrijf biedt kleinere canuleformaten voor premature pasgeborenen en kinderen van verschillende leeftijden tot canules voor volwassenen. Elke canule moet goed in de neus van de patiënt passen en voorkomt dat er lucht in de kamer rond de canule kan stromen, wat met standaard neuscanules kan gebeuren. Elke fabrikant heeft ook een maximumdebiet voor elke maat canule, afhankelijk van de grootte en leeftijd van de patiënt.
Elk bedrijf biedt kleinere canuleformaten voor premature pasgeborenen en kinderen van verschillende leeftijden tot canules voor volwassenen. Elke canule moet goed in de neus van de patiënt passen en voorkomt dat er lucht in de kamer rond de canule kan stromen, wat met standaard neuscanules kan gebeuren. Elke fabrikant heeft ook een maximumdebiet voor elke maat canule, afhankelijk van de grootte en leeftijd van de patiënt.
Hoe het werkt:
Verwarmde &Vochtige:
Verwarmde en bevochtigde zuurstof heeft een aantal voordelen in vergelijking met standaardzuurstoftherapie. Standaard zuurstoftherapie die via een neuscanule of een ander apparaat, zoals een non-rebreather, wordt toegediend, is koud (niet verwarmd) en droog (niet bevochtigd). Dit kan leiden tot luchtwegontsteking, waardoor de luchtwegweerstand kan toenemen en de mucociliaire functie kan afnemen, wat kan leiden tot een verminderde secretieklaring (1). Ook kan een aanzienlijke hoeveelheid calorieën worden verbruikt bij individuen om gas zowel op te warmen als te bevochtigen tijdens een normale ademhaling (2).
HFNC kan gas verwarmen (tot 37oC) en bevochtigen, wat luchtwegontsteking kan verminderen, mucociliaire functie in stand kan houden, slijmklaring kan verbeteren en het calorieverbruik bij acuut respiratoir falen kan verminderen (1-2).
Inspiratoire eisen:
Een voor de hand liggend voordeel, maar het vermelden waard, is dat een hoge flow een zeer hoge gasstroom kan geven. Dit is belangrijk omdat patiënten met acuut ademhalingsfalen extreem tachypneus kunnen zijn, waardoor hun piek inspiratoire flow, die normaal 30L/min – 60L/min kan zijn, kan oplopen tot 120 L/min (3). Dus als u uw tachypneuze patiënt met een PIF rate van 120L/min en een minuutvolume >20L/min op een 15L/min NRB masker plaatst, helpt u hem misschien niet zo veel als u denkt. Ik ga een beetje later in dit overzicht op dit punt in wanneer we het concept van zuurstofverdunning bespreken.
Functionele Restcapaciteit:
Je hebt misschien gezocht naar het opsommingsteken dat zegt dat Hi Flow PEEP biedt en je kunt het niet vinden? Er is enige discussie geweest over de vraag hoeveel PEEP een hoogdebiettoestel kan leveren. HFNC is aangetoond tot 1 mm van Hg van PEEP te leveren voor elke 10L / min van de stroom geleverd met gesloten mond ademhaling. (4-5)
Ik ben er niet zeker van dat dit voor alle patiënten geldt, en wel omdat er veel factoren zijn die van invloed kunnen zijn op de hoeveelheid PEEP die daadwerkelijk aan een patiënt kan worden toegediend. Factoren zoals de grootte van de patiënt (zwaarlijvig, volwassen, kind), de liter flow die wordt toegediend (L/Min), en mond open versus mond dicht ademen (druk kan ontsnappen wanneer een patiënt zijn mond open heeft) kunnen allemaal van invloed zijn op de hoeveelheid PEEP die wordt toegediend (4)
De discussie kan doorgaan, maar het lijkt erop dat HFNC het functioneel restvolume (FRC) van een patiënt kan verhogen, of het longvolume aan het eind van de uitademing, iets wat PEEP meestal verbetert. Een studie van Riera J. et al toonde aan dat het gebruik van HFNC de End Expiratory Lung Impendence (EELI) deed toenemen, wat een verbetering van de FRC impliceert (6). Zij gebruikten elektrische impedantietomografie (EIT), een niet-invasieve, real-time beeldvormingsmethode die een dwarsdoorsnede van de long geeft om een verhoogde end-exiratoire longafhankelijkheid (EELI) aan te tonen.
Het lijkt er ook op dat het gebruik van HFNC de voorspanning kan verlagen door de intra-thoracale druk te verhogen, ook een kenmerk dat gewoonlijk aan PEEP wordt toegeschreven. Roca et al toonden in een sequentiële intervalstudie bij 10 patiënten (NYHA III hartfalen, maar niet in een acute CHF exacerbatie) aan dat het gebruik van Hi Flow inspiratoire collaps van de vena cava inferior (IVC) veroorzaakte ten opzichte van de uitgangswaarde van de patiënt gemeten met echocardiogram (7).
Hi flow lijkt alveolaire rekrutering en verhoogde FRC te veroorzaken, evenals verhoging van de intrathoracale druk, waarschijnlijk als gevolg van toegevoegde PEEP, maar het is niet zeker of misschien een ander mechanisme verantwoordelijk kan zijn voor deze bevindingen.
Lichter:
Patiënten geven vaak de voorkeur aan het gebruik van HFNC boven dat van niet-invasieve positieve-drukbeademing (CPAP of BPAP), omdat het nauwsluitende masker voor sommige patiënten oncomfortabel kan zijn. Ze kunnen er zelfs de voorkeur aan geven boven standaard NC omdat de verwarmde, bevochtigde gassen hun mucosa niet uitdrogen zoals bij standaard zuurstoftherapie (5). Dit kan leiden tot een hogere therapietrouw bij HFNC en misschien tot een verbetering van de oxygenatie en het ademwerk van uw patiënt.
O2 Verdunning:
Ik leerde op mijn ICU-rotatie als stagiair dat elke 1 liter neuscanule ~4% fiO2 boven kamerlucht (21%) zal leveren. Dus 1 liter/min via de NC zou ~ 25% fi02 moeten leveren, en 2 liter/min zou 29% fiO2 moeten leveren (zie tabel 1 hieronder). Ik heb jarenlang geloofd dat deze “1:4 regel” waar was, maar laten we eens kijken of hij zinvol is voor een patiënt in acute ademnood

Stel u een man voor van 70 kg die 30-40 bpm ademt met normale ademhalingsvolumes (~500 ml) en een zekere hypoxemie ontwikkelt. De minuutbeademing van deze patiënt zou tussen 15-20 liter/minuut liggen. U besluit deze patiënt op 6 liter per minuut NC te plaatsen, wat theoretisch een fiO2 van 45% zou moeten opleveren (6 liter x 4% = 24 + kamerlucht (21%) = 45%) als de “1:4 regel” geldt. Als deze patiënt 15-20 liter via de mond en via de neus (rond de neuscanule) ademt bij 21%, denkt u dan dat deze patiënt daadwerkelijk 45% fiO2 aan de luchtpijp krijgt toegediend?
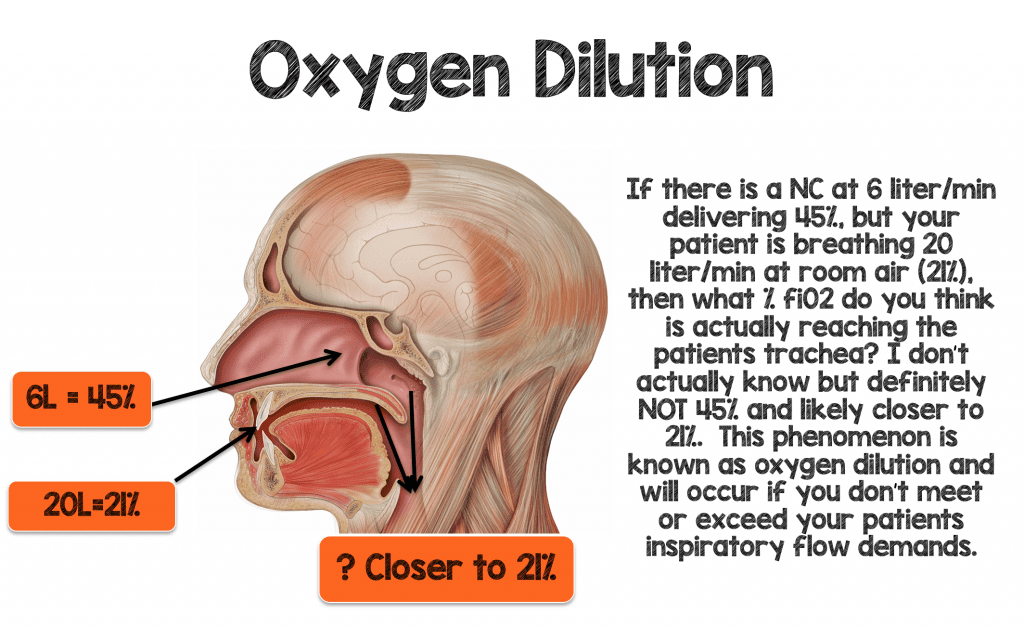
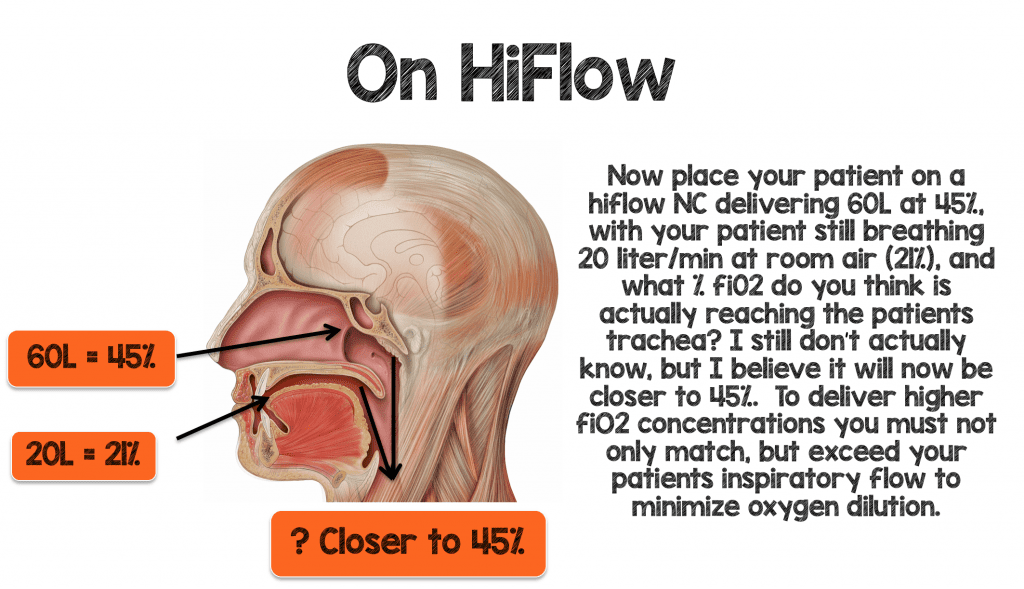
Om de patiënt effectief hogere hoeveelheden fiO2 te kunnen toedienen, moet u de minutenlange ventilatie en inspiratoire behoefte van de patiënt niet alleen evenaren, maar zelfs overtreffen om de zuurstofverdunning te minimaliseren.
Uitwaseming van dode ruimte:
Wij ademen normaal gesproken een derde van ons eerder uitgeademde getijdevolume opnieuw in en in plaats van 21% (kamerlucht) en verwaarloosbare hoeveelheden kooldioxide, ademen we misschien wel 15-16% zuurstof en 5-6% kooldioxide opnieuw in. Dit komt doordat de eerder uitgeademde lucht (met een laag zuurstofgehalte en wat kooldioxide) niet volledig wordt uitgeademd en in de bovenste luchtwegen achterblijft. Wanneer de patiënt zijn volgende ademhaling uit atmosferisch gas haalt, komt niet al dat gas in de longblaasjes. In feite is het een mengsel van het nieuwe atmosferische gas (21% 02, verwaarloosbaar CO2) en hun eerder uitgeademde gas (<21% zuurstof en wat CO2). Bij patiënten met acute ademhalingsmoeilijkheden wordt het percentage gas dat we herinademen groter, en als gevolg daarvan kunnen we grotere hoeveelheden kooldioxide herinademen omdat we onze ademhalingen uit een gemengd reservoir uit onze bovenste luchtwegen halen. Een andere manier om dit te zeggen is dat onze dode ruimte toeneemt bij acuut ademfalen.
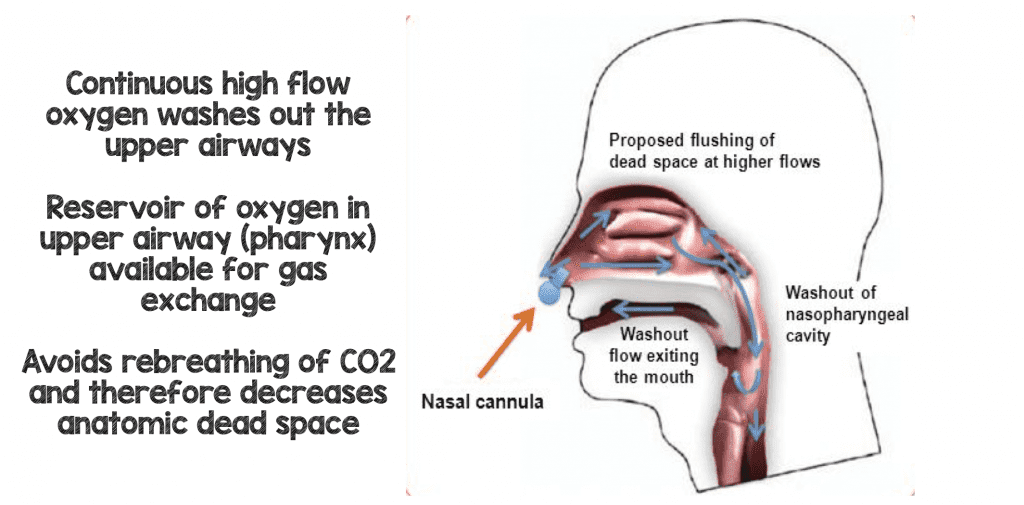
Een van de belangrijkste voordelen van HFNC (sommigen beweren dat dit zelfs het belangrijkste voordeel is) is dat u een continue stroom vers gas met hoge stroomsnelheden krijgt die de dode ruimte in de keelholte van de patiënt (het oude gas met een laag zuurstofgehalte en een hoog CO2-gehalte) vervangt of uitspoelt. Bij elke ademhaling die de patiënt nu opnieuw uitblaast, wordt kooldioxide uitgespoeld en vervangen door zuurstofrijk gas, waardoor de ademhalingsefficiëntie wordt verbeterd (8).

Guest Post Co-Written By

Thomas Lettich, D.O.
Internal Medicine/Pediatrics Resident Physician
Geisinger Medical Center
Danville, Pennsylvania
- Chidekel, A et al. The Effects of Gas Humidification with High-Flow Nasal Cannula on Cultured Human Airway Epithelial Cells. Longgeneeskunde 2012. PMID: 22988501
- Dysart, K et al. Onderzoek in High Flow Therapy: Werkingsmechanismen. Respiratoire geneeskunde 2009. PMID: 19467849
- Katz, JA et al. Inspiratory Work with and Without Continuous Positive Airway Pressure in Patients with Acute Respiratory Failure. Anesthesiologie 1985. PMID: 3904528
- Parke R et al. Pressures delivered by Nasal High Flow Oxygen During all Phases of the Respiratory Cycle. Respiratoire zorg 2013. PMID: 23513246
- Frat JP et al. High-Flow Nasal Oxygen Therapy and Noninvasive Ventilation in the Management of Acute Hypoxemic Respiratory Failure. Annals of Translational Medicine 2017). PMID: 28828372
- Riera J et al. Effect of High-Flow Nasal Cannula and Body Position on End-Expiratory Lung Volume: A Cohort Study Using Electrical Impedance Tomography. Respiratoire geneeskunde 2013. PMID: 23050520
- Roca O et al. Patiënten met New York Heart Association klasse III hartfalen kunnen baat hebben bij ondersteunende therapie met High Flow Nasal Cannula: High Flow Nasal Cannula in Heart Failure. Journal Crit Care 2013. PMID: 23602035
- Möller W et al. Nasal High Flow Clears Anatomical Dead Space in Upper Airway Models. Tijdschrift voor toegepaste fysiologie 2015). PMID: 25882385
Steun de show door te betalen & Claiming 0.5hrs of CME/CEH door op het onderstaande logo te klikken

Post Peer Reviewed By: Salim R. Rezaie, MD (Twitter: @srrezaie)
- Bio
- Laatste berichten
Frank Lodeserto MD
Laatste berichten van Frank Lodeserto MD (zie alle)
- De RELAx Trial: Wat is de optimale PEEP bij patiënten zonder ARDS? – 1 februari 2021
- COVID-19 Update: Het COVID-19-vaccin van Pfizer – 15 december 2020
- Hemofagocytische lymfohistiocytose (HLH): A Zebra Diagnosis We Should All Know – July 30, 2020