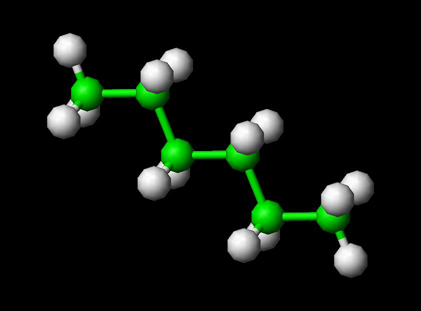
Aby zobaczyć molekułę heksanu w 3D —->zapoznaj się z programem Jsmol
.>> w 3D z Jsmol
Właściwości chemiczne i fizyczne cząsteczki heksanu
Heksan jest węglowodorem alkanowym o wzorze chemicznym CH3(CH2)4CH3. Przedrostek „hex” odnosi się do jego sześciu węgli, podczas gdy końcówka „ane” wskazuje, że jego węgle są połączone wiązaniami pojedynczymi. Izomery heksanu są w dużej mierze niereaktywne i są często stosowane jako obojętny rozpuszczalnik w reakcjach organicznych, ponieważ są bardzo niepolarne. Są one również powszechnymi składnikami benzyny i klejów używanych do produkcji butów, wyrobów skórzanych i pokryć dachowych. Dodatkowo, jest stosowany w rozpuszczalnikach do ekstrakcji olejów do gotowania oraz jako środek czyszczący w produkcji obuwia, mebli i tekstyliów.
Produkcja
Heksan jest produkowany w procesie rafinacji ropy naftowej. Dokładny skład frakcji zależy w dużej mierze od źródła pochodzenia ropy (surowa lub reformowana) i ograniczeń rafinacji. Produktem przemysłowym (zwykle około 50% masy izomeru prostego) jest frakcja wrząca w temperaturze 65-70 °C.
Toksyczność
Toksyczność ostra heksanu jest stosunkowo niska, chociaż jest on łagodnym środkiem znieczulającym. Wdychanie wysokich stężeń wywołuje najpierw stan łagodnej euforii, a następnie senność z bólami głowy i mdłościami.
Przewlekłe zatrucie heksanem obserwowano u osób nadużywających rozpuszczalników rekreacyjnie oraz u pracowników przemysłu obuwniczego, renowacji mebli i budowy samochodów. Początkowe objawy to mrowienie i skurcze w rękach i nogach, a następnie ogólne osłabienie mięśni. W ciężkich przypadkach obserwuje się zanik mięśni szkieletowych, utratę koordynacji i problemy z widzeniem.
Podobne objawy obserwuje się w modelach zwierzęcych. Wiążą się one z degeneracją obwodowego układu nerwowego (i ostatecznie ośrodkowego układu nerwowego), począwszy od dystalnych części dłuższych i szerszych aksonów nerwowych. Toksyczność nie jest spowodowana przez sam heksan, ale przez jeden z jego metabolitów, heksan-2,5-dion. Uważa się, że reaguje on z grupą aminową łańcucha bocznego reszt lizyny w białkach, powodując ich usieciowanie i utratę funkcji białek.
Skutki zatrucia heksanem u ludzi są niepewne. W 1994 r. n-heksan został włączony do wykazu substancji chemicznych na liście Toxic Release Inventory (TRI).W drugiej części XX i na początku XXI wieku wiele eksplozji zostało przypisanych spalaniu gazu heksanowego. W 2001 r. Amerykańska Agencja Ochrony Środowiska wydała przepisy dotyczące kontroli emisji heksanu ze względu na jego potencjalne właściwości rakotwórcze i obawy związane z ochroną środowiska.
Zastosowanie
W przemyśle, heksany są stosowane w produkcji klejów do butów, wyrobów skórzanych i pokryć dachowych. Stosuje się je również do ekstrakcji olejów spożywczych (takich jak olej rzepakowy lub sojowy) z nasion, do oczyszczania i odtłuszczania różnych przedmiotów oraz w produkcji wyrobów włókienniczych. Jest on powszechnie stosowany w Stanach Zjednoczonych do ekstrakcji oleju sojowego na bazie żywności i stanowi zanieczyszczenie potencjalnie obecne we wszystkich produktach spożywczych z soi przy użyciu tej techniki, która w kontrowersyjny sposób nie jest regulowana przez FDA.
Typowym laboratoryjnym zastosowaniem heksanów jest ekstrakcja zanieczyszczeń olejowych i tłuszczowych z wody i gleby do analizy. Ponieważ heksan nie może być łatwo zdeprotonowany, jest on używany w laboratorium do reakcji, które obejmują bardzo silne zasady, takie jak przygotowanie organolitów. Na przykład, butyllit jest zwykle dostarczany jako roztwór heksanu.
Heksany są powszechnie stosowane w chromatografii jako rozpuszczalnik niepolarny. Wyższe alkany obecne jako zanieczyszczenia w heksanach mają podobne czasy retencji jak rozpuszczalnik, co oznacza, że frakcje zawierające heksan będą również zawierać te zanieczyszczenia. W chromatografii preparatywnej, zatężanie dużej objętości heksanów może prowadzić do otrzymania próbki, która jest znacznie zanieczyszczona alkanami. Może to spowodować, że związek stały zostanie otrzymany jako olej, a alkany mogą zakłócać analizę.
W wielu zastosowaniach (zwłaszcza farmaceutycznych) wycofuje się stosowanie n-heksanu ze względu na jego długotrwałą toksyczność. Jest on często zastępowany przez n-heptan, który nie tworzy toksycznego metabolitu heksan-2,5-dionu.
Zobacz także:
.