Karthish Manthiram marzy o zelektryfikowanej przyszłości. Inżynier chemik z MIT należy do rosnącej grupy naukowców badających sposoby, w jakie elektrochemia zasilana energią odnawialną mogłaby zastąpić paliwa kopalne jako podstawę przemysłu chemicznego.
’Ogólna wizja to myślenie o przyszłości, w której produkcja chemiczna zaczyna się tylko od dwutlenku węgla, wody i azotu', mówi Manthiram. Jeśli zaczniemy od tych trzech surowców i będziemy dysponować odnawialną energią elektryczną, możemy wyobrazić sobie wykorzystanie dwutlenku węgla jako źródła atomu węgla, wody jako źródła oksygenów i hydrogenów oraz dinitrogenu jako źródła azotu i zacząć zszywać stosunkowo złożone cząsteczki organiczne” – mówi.
W tym przyszłym świecie, o którym marzymy, moglibyśmy wytwarzać amoniak z powietrza, wody i odnawialnej energii elektrycznej
Najwyżej na liście cząsteczek, które badacze elektrochemii chcą wytwarzać w ten sposób, znajduje się amoniak. Jako kluczowy składnik nawozów syntetycznych, rocznie produkuje się około 175 milionów ton amoniaku. Jednak ogromne ilości, w jakich jest on wytwarzany, oraz energochłonny charakter jego produkcji oznaczają, że zakłady produkujące amoniak zużywają około 2% globalnej produkcji energii i wytwarzają podobną część globalnej emisji dwutlenku węgla.
Wraz z szybko rosnącą dostępnością odnawialnej energii elektrycznej naukowcy widzą alternatywną drogę do uzyskania amoniaku. 'W tym przyszłym świecie, o którym marzymy, moglibyśmy wytwarzać amoniak tylko z powietrza, wody i odnawialnej energii elektrycznej' – mówi Manthiram. W tym roku laboratorium Manthirama dołączyło do garstki na całym świecie, które ostatecznie wykazały, że przy udziale elektrokatalizatora litowego, amoniak może być wytwarzany w ten sposób.
W młodej dziedzinie badań, w której wczesne twierdzenia o elektrochemicznej produkcji amoniaku często nie wytrzymywały kontroli, garstka solidnych wyników dotyczących produkcji amoniaku przy udziale litu może stanowić solidną podstawę, na której zaczyna się budować czystą przyszłość amoniaku.
Podzielony ból głowy
Wielkim wyzwaniem w syntezie amoniaku, elektrochemicznej lub innej, jest wymóg wzięcia dwutlenku węgla z powietrza i podzielenia go na dwie części. Potrójne wiązanie łączące dwa atomy azotu jest jednym z najsilniejszych znanych.
Przez ostatnie stulecie zakłady produkujące amoniak przezwyciężyły niechęć dwutlenku węgla do reagowania w dwuetapowym procesie. W pierwszym etapie, reakcji reformingu parowo-metanowego, woda i metan są podgrzewane nad katalizatorem, który zachęca do zamiany partnerów atomowych, wytwarzając strumień dwutlenku węgla i wodoru. Wodór jest następnie poddawany reakcji z azotem za pomocą katalizatora żelaznego w procesie Habera-Boscha, nazwanym tak na cześć niemieckich chemików Fritza Habera, który wynalazł tę reakcję, i Carla Boscha, który udoskonalił ją dla przemysłu.
Duża część naszych nierówności w dostępie do żywności na świecie wynika z faktu, że produkcja amoniaku jest scentralizowana
To, co odkrył Haber, było sposobem na obejście problemu, że, w wysokich temperaturach potrzebnych do rozdzielenia dinitrogenu, równowaga dla tworzenia amoniaku leży daleko w lewo, mówi Ib Chorkendorff, badacz katalizy na Uniwersytecie Technicznym w Danii i dyrektor Centrum Villum dla nauki o zrównoważonych paliwach i chemikaliach. Wielkim wynalazkiem Habera było uświadomienie sobie, że nie otrzymamy żadnego amoniaku, jeśli nie poddamy go ciśnieniu”, mówi Chorkendorff. Jeśli weźmiesz cztery mole gazu i zamienisz je w dwa, ciśnienie bardzo pomaga”. Dzisiejsze zakłady Haber Bosch pracują zazwyczaj pod ciśnieniem przekraczającym 200 atmosfer.
Stechiometryczny dwutlenek węgla, który powstaje w wyniku reakcji, a także emisja dwutlenku węgla związana z wytwarzaniem wymaganych wysokich temperatur i ciśnień, to jeden z istotnych powodów, aby szukać alternatywnego podejścia. Ale nawet gdyby dwutlenek węgla nie był gazem zatrzymującym promieniowanie podczerwone, co prowadzi do globalnego ocieplenia, nadal mielibyśmy problem z tym procesem” – mówi Manthiram. Naprawdę wysokie temperatury i ciśnienia oznaczają, że po prostu nie jest możliwe przeprowadzenie tej reakcji w sposób rozproszony.'
Koszty budowy reaktorów wysokociśnieniowych przesuwają równowagę ekonomiczną w kierunku budowy bardzo dużych, scentralizowanych zakładów amoniaku. Duża część naszych nierówności w dostępie do żywności na świecie wynika z faktu, że produkcja amoniaku jest scentralizowana” – mówi Manthiram. W Afryce Subsaharyjskiej infrastruktura dystrybucji jest tak słaba, że nawóz kosztuje od dwóch do trzech razy więcej niż średnia międzynarodowa. Ogranicza to jego wykorzystanie, co prowadzi do niskich plonów, głodu, niższej wydajności siły roboczej, niższych zarobków, co jeszcze bardziej ogranicza zdolność do pokrycia kosztów nawozu. Jest to ogromny problem do rozwiązania.”
Ammoniak wytwarzany z powietrza, wody i odnawialnej energii elektrycznej, w temperaturach i ciśnieniach otoczenia, mógłby być produkowany wszędzie tam, gdzie jest potrzebny.
Poczucie atrakcyjności odnawialnych źródeł energii
Badacze od dziesięcioleci próbują znaleźć bardziej ekologiczne alternatywy dla reakcji Habera-Boscha. Tym razem różnica polega na szybko zmieniającym się rynku energetycznym, mówi Doug MacFarlane, chemik z Uniwersytetu Monash, który kieruje Centrum Doskonałości w Nauce o Elektromateriałach przy Australijskiej Radzie ds. W ciągu ostatnich około 10 lat dostępne stały się coraz większe ilości coraz tańszej energii odnawialnej” – mówi MacFarlane. Od 2010 roku cena energii słonecznej spadła o 80%, a energii wiatrowej o 50%, z perspektywą dalszych spadków. 'To sprawiło, że skupiono się na technologiach elektrochemicznych w bardzo szerokim zakresie, wykorzystując elektrony jako ostateczny reduktant', mówi.

Źródło: Dzięki uprzejmości Science and Technology Facilities Council
Siemens Energy Green Ammonia Demonstrator w Wielkiej Brytanii testuje rozszczepianie wody i chemię Habera-Boscha
Laboratorium MacFarlane’a – podobnie jak wiele laboratoriów syntezy elektrochemicznej – początkowo koncentrowało się na chemii rozszczepiania wody napędzanej źródłami odnawialnymi, w celu wytworzenia strumienia czystego wodoru, który mógłby być wykorzystywany jako surowiec lub paliwo. Druga fala badań koncentrowała się na redukcji dwutlenku węgla, aby przekształcić emisje dwutlenku węgla w użyteczne produkty – mówi. Wyrastając z tego, jakieś sześć lat temu zaczęliśmy zdawać sobie sprawę, że nasze badania mają jeszcze trzecią perspektywę, a mianowicie redukcję azotu” – mówi MacFarlane. To te same pomysły, ten sam zestaw laboratoryjny, ale inny substrat i produkt docelowy”. Zamiast wodoru, ogniwo produkowałoby strumień amoniaku.
Produkcja amoniaku mogłaby wykraczać daleko poza wykorzystanie nawozów. Spadające ceny energii elektrycznej napędzane przez odnawialne źródła energii już spowodowały ponowne przemyślenie tradycyjnej reakcji reformingu parowego (patrz ramka Reforming elektryczny poniżej). Kraje takie jak Australia, które posiadają zasoby energii słonecznej i wiatrowej znacznie przekraczające ich własne potrzeby, zwracają uwagę na elektrochemicznie syntetyzowany amoniak nie tylko do czystszej produkcji nawozów, ale jako zielone paliwo, które mogłoby umożliwić eksport energii odnawialnej.
W maju 2020 roku MacFarlane i jego koledzy opublikowali mapę drogową określającą potencjalną drogę do zielonej gospodarki amoniakalnej. Koncepcja pierwszej generacji, polegająca na połączeniu konwencjonalnej produkcji amoniaku z wychwytywaniem dwutlenku węgla, jest już wypierana przez podejście drugiej generacji, w którym wodór dla Haber-Bosch pochodzi z zasilanego energią odnawialną elektrochemicznego rozszczepiania wody, a nie z reformingu parowego napędzanego metanem.
Po dziesięcioleciach badań elektrochemiczne rozszczepianie wody osiągnęło punkt, w którym dostępne stają się urządzenia do rozszczepiania wody na skalę przemysłową, takie jak ITM-Power w Wielkiej Brytanii i Siemens w Niemczech. Siemens przetestował już koncepcję połączenia technologii rozszczepiania wody i Haber-Boscha w demonstracyjnym zakładzie Siemens Green Ammonia Demonstrator w Oxfordshire. W regionie Pilbara w Zachodniej Australii – który otrzymuje jedne z najwyższych rocznych ilości energii słonecznej na całej planecie – Yara Fertilisers również przygotowuje się do pilotażowego przejścia. Zakład ten produkuje obecnie 5% światowej produkcji amoniaku.
Główną barierą dla szerokiego rozpowszechnienia produkcji amoniaku drugiej generacji nie jest już koszt odnawialnej energii elektrycznej, mówi MacFarlane. Barierą jest koszt kapitałowy ogniw elektrolizy”, mówi. Najlepiej działające elektrody do rozszczepiania wody wykorzystują metale szlachetne.
Reformacja elektryczna
Pierwszym krokiem w konwencjonalnej syntezie amoniaku jest wytworzenie wodoru, który zostanie połączony z dwutlenkiem węgla w celu wytworzenia amoniaku. Obecnie wodór ten pochodzi z metanu, poprzez reakcję reformingu parowego, napędzanego przez szereg palników gazowych otaczających pokryte katalizatorem rury, w których zachodzi reakcja.
Ilość katalizatora może być zredukowana o rząd wielkości
Reforming parowy jest tak endotermiczny, generuje znaczny gradient temperatury wewnątrz rury, co może prowadzić do odkładania się węgla na powierzchni katalizatora i zablokowania lub nawet pęknięcia rury.
W 2019 roku Chorkendorff wykazał, że reakcja może być znacznie skuteczniej napędzana przez ogrzewanie omowe. Przepuszczanie prądu elektrycznego przez stalową rurę reformera parowego generuje ciepło in situ, ze względu na oporność elektryczną. Uzyskujemy bardzo bliski kontakt pomiędzy źródłem ciepła a katalizatorem, co eliminuje wszystkie problemy związane z transportem ciepła i nie mamy żadnego gradientu temperatury' – mówi Chorkendorff.
Oprócz unikania osadzania się węgla, ogrzewanie omowe ma wiele zalet, dodaje Chorkendorff. Uruchomienie instalacji do reformingu parowego zajmuje zwykle około tygodnia, ale system z ogrzewaniem omowym zajmuje około dwóch minut. Ilość katalizatora można zredukować o rząd wielkości, a wielkość instalacji o dwa rzędy wielkości” – mówi. Wcześniej koszty energii elektrycznej sprawiały, że ogrzewanie omowe było nieopłacalne – ale dzięki odnawialnym źródłom energii, jak twierdzi Chorkendorff, nie jest to już problemem. Firma, z którą Chorkendorff nawiązał współpracę w celu przeprowadzenia badań, pracuje już nad instalacją pilotażową i ma plany dotyczące ogrzewania omowego wykraczające daleko poza reforming parowy, mówi.
Obniżanie kosztów
Znalezienie tańszych alternatyw dla elektrod platynowych i irydowych było długoterminowym celem laboratorium Chorkendorfa. W 2005 roku zespół wykazał, siarczek molibdenu sprawia, że silny elektrokatalizator dla reakcji ewolucji wodoru. Katalitycznie aktywna część MoS2 okazało się być wzdłuż krawędzi katalizatora, a nie jego płaskiej powierzchni, co skłoniło wiele badań do opracowania nanostrukturalnych lub warstwowych materiałów MoS2, które maksymalizują udział krawędzi.
Wiemy, że katalizator OER musi być tlenkiem i musi być stabilny w ekstremalnych wartościach pH
’Przyjrzeliśmy się dużo ewolucji wodoru, ale uważamy to za rozwiązane – istnieje kilka bardzo dobrych katalizatorów' – mówi Chorkendorff. 'Prawdziwym problemem jest energia tracona z powodu ewolucji tlenu', argumentuje. Ogniwa rozszczepiające wodę produkują wodór na katodzie i tlen na anodzie (patrz ramka Tymczasem, na anodzie poniżej). Niska wydajność po stronie reakcji ewolucji tlenu (OER) w ogniwie wodnym sprawia, że cały proces jest bardziej energochłonny i droższy w eksploatacji. 'Dziś działają one z wydajnością maksymalnie 70%, ale normalnie nie jest ona tak wysoka.'
Pomimo lat pracy, przełom w katalizatorze OER ma dopiero nadejść. Nic nie wskazuje na to, że nie znajdziemy materiału, ale wiemy, że jest on coraz trudniejszy – wiemy, że musi to być tlenek, musi być stabilny albo w silnym kwasie, albo w silnym roztworze zasadowym” – mówi Chorkendorff. Elektrolizery pracują na jednym lub drugim biegunie skali pH, aby zmaksymalizować wydajność, ale najbardziej aktywne katalizatory OER nie są wystarczająco stabilne w tych warunkach, aby można je było stosować w praktyce przez długi czas.
Jedną z koncepcji, wprowadzoną przez Daniela Nocerę, pracującego wówczas w Massachusetts Institute of Technology w USA, są samoregenerujące się katalizatory OER, które tworzą się in-situ i nieustannie regenerują się z jonów metali w elektrolicie. Elektrokatalizatory Nocery działały w warunkach neutralnych. W 2019 r. MacFarlane i jego współpracownicy zademonstrowali samoregenerujący się, generowany in situ katalizator OER z mieszanego tlenku metalu do pracy w warunkach silnie kwaśnych.
W międzyczasie na anodzie
W przypadku większości procesów elektrochemicznych – wytwarzania wodoru lub amoniaku, albo redukcji dwutlenku węgla – wszystkie oczy skierowane są na katodę. Reakcja towarzysząca zachodząca na anodzie jest procesem utleniającym, który zazwyczaj generuje tlen, niewinny produkt uboczny głównego procesu.
’Wiele osób uważa tlen za produkt odpadowy', mówi Chorkendorff. Ale gaz ten ma potencjalnie wartościowe zastosowania. Strumień czystego tlenu jest kluczem do koncepcji elektrowni tlenowo-paliwowych, które omijają problemy związane z wychwytywaniem dwutlenku węgla poprzez spalanie paliwa w tlenie, a nie w powietrzu. Jeśli spalisz biomasę w elektrowni z tym tlenem, otrzymasz znacznie wyższą klasę dwutlenku węgla', mówi Chorkendorff.
Manthiram również widzi wartość w reakcji anodowej. Pracujemy nad metodami, dzięki którym można wykorzystać ten tlen do syntezy chemicznej, zamiast próbować łączyć dwa atomy tlenu, aby uzyskać dwutlenek węgla, co jest kinetycznie trudne do wykonania. Z wcześniejszych prac, zespół wiedział, że tlenek manganu jest katalizatorem, który utlenia wodę, generując w procesie gatunek mangan oxo. Co by się stało, gdybyśmy mogli przechwycić ten proces przy użyciu olefiny, aby stworzyć epoksyd? pyta Manthiram. To były tylko przypuszczenia, ale jakoś się udało”. Oprócz produkcji epoksydów, zespół pokazał, że może wstawić tlen do wiązania węgiel-węgiel, aby stworzyć laktony. 'To może sprawić, że elektrolizer wody będzie bardziej ekonomicznie opłacalny', mówi Manthiram. 'Nie ma sposobu, aby zrobić cały światowy wodór w ten sposób – mamy o wiele za duże zapotrzebowanie na wodór – ale moglibyśmy zrobić trochę wodoru, który jest naprawdę tani podczas współtworzenia laktonów, które trafiają do biodegradowalnych tworzyw sztucznych o dużej objętości lub epoksydów o dużej objętości, aby zrobić glikol etylenowy.'
Niezawodne źródła
Przy rozszczepianiu wody, które wciąż nie zostało udoskonalone i przy ciągłej zależności od reakcji Habera-Boscha, istnieje nadzieja, że produkcja zielonego amoniaku drugiej generacji jest krokiem w kierunku ostatecznego celu, jakim jest produkcja amoniaku bezpośrednio za pomocą środków elektrochemicznych. Zamiast produkować dwuwodny gaz, atomy wodoru i azotu mogłyby być łączone in situ na katodzie w celu wytworzenia amoniaku.
Głównym wyzwaniem jest znalezienie sposobu na uprzywilejowanie produkcji amoniaku w stosunku do tworzenia dwuwodoru, wyjaśnia Manthiram. Rezerwuar elektronów na katodzie mógłby reagować z dwoma protonami w roztworze, aby wytworzyć wodór; lub zamiast tego reagować z azotem, aby przerwać potrójne wiązanie, a także zwerbować sześć protonów, aby wytworzyć dwie cząsteczki amoniaku' – mówi Manthiram. Praktycznie każdy katalizator będzie miał tendencję do wytwarzania większej ilości wodoru niż amoniaku.'
W ciągu ostatnich około pięciu lat pojawił się strumień prac, które zdawały się pokazywać katalizatory mogące wytworzyć trochę amoniaku w przeważającym strumieniu wodoru wytwarzanego na katodzie. W międzyczasie, laboratorium MacFarlane’a testowało pomysł, że dobrym sposobem na ograniczenie produkcji wodoru byłoby wyeliminowanie jednego głównego źródła protonów – elektrolitu. Przechodząc na aprotyczny elektrolit w postaci cieczy jonowej, a następnie dodając tylko kontrolowaną ilość wody, kwasu lub zasady, zespół wykazał, że może sprzyjać produkcji amoniaku.
Praktycznie każdy katalizator będzie miał tendencję do wytwarzania więcej wodoru niż amoniaku
’Praca aprotyczna jest dość agnostyczna w odniesieniu do katalizatora, więc nasze podejście zawsze polegało na zastosowaniu jej do najlepszego katalizatora, jaki mogliśmy znaleźć' – mówi MacFarlane. Ilekroć ukazywała się praca na temat nowego katalizatora, szybko staraliśmy się powtórzyć jej wyniki w literaturze, a następnie zastosować ją w naszej pracy aprotycznej. Z pewną frustracją, w niektórych przypadkach po rozmowach z autorami, nigdy nie udało nam się sprawić, by katalizator z literatury działał dobrze. W końcu staliśmy się ekspertami od tego, co nie działa.”
Ale przekształcanie azotu w amoniak jest bardzo trudne, zbyt łatwo jest wytworzyć śladowe ilości amoniaku z innych źródeł azotu. Długa lista możliwych źródeł przypadkowego azotu obejmuje elektrodę lub ślady NO lub NO2 w gazie azotowym. Usuń lub uwzględnij te źródła, a ilość azotu przekształcanego w amoniak przez większość systemów katalizatorów jest tak niska, że nie ma znaczenia praktycznego, mówi MacFarlane.
' jest wielkim zwolennikiem sprawdzenia, skąd właściwie pochodzi amoniak i czy katalizator rzeczywiście wykonuje pracę' – mówi Lauren Greenlee z Uniwersytetu Arkansas w USA, która jako jedna z pierwszych pracowała nad elektrokatalityczną produkcją amoniaku i jako jedna z pierwszych podkreśliła, że przypadkowy amoniak jest poważnym problemem. 'Bezpośrednie przekształcenie dinitrogenu w dwie cząsteczki amoniaku na powierzchni katalizatora jest po prostu bardzo trudnym problemem i nie wiem, czy jesteśmy tak blisko jego rozwiązania.'
Na razie Greenlee wycofał się z eksperymentów związanych z produkcją amoniaku, aby przeprowadzić bardziej fundamentalne badania nad tym problemem. Zainteresowaliśmy się chemią elektrolitów i pracujemy nad zrozumieniem chemii powierzchni katalizatora i tego, jak zmienia się ona w tych elektrolitach' – mówi Greenlee. 'Nie składam żadnych obietnic dotyczących wytwarzania amoniaku, ale mam nadzieję, że dowiemy się wiele o katalizatorze i wniesiemy wkład w tę dziedzinę.'
Patrząc na lit
Tak samo jak Greenlee i MacFarlane, Chorkendorff określił rygorystyczne eksperymenty kontrolne, w tym z użyciem radioznakowanego dinitrogenu, potrzebne do wykazania, że wytwarzany amoniak rzeczywiście pochodzi z dinitrogenu, a nie z alternatywnego źródła azotu. Opublikowaliśmy metodę, ponieważ mam już dość oglądania tych wszystkich prac, w których twierdzą, że wytwarzają amoniak, ponieważ nie wytwarzają go wcale' – mówi Chorkendorff. 'Znam tylko jeden system, który na pewno wytwarza amoniak, i jest to szlak z udziałem litu.'
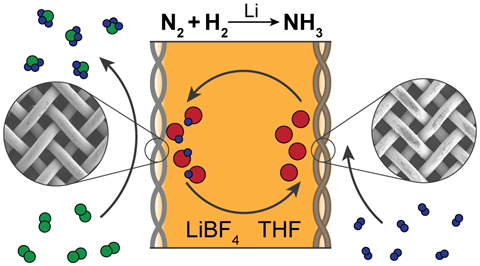
Źródło: © Nikifar Lazouski et al/Springer Nature Limited 2020
Katalizatory na bazie litu wydają się być najlepszym systemem, jak w tym opracowanym przez grupę Karthisha Manthirama z MIT
Lit jest jedynym metalem, który może spontanicznie reagować z dinitrogenem, tworząc azotek metalu – przerywając potrójne wiązanie dinitrogenu w procesie. Zdolność litu do generowania amoniaku została zademonstrowana przez japońskich badaczy w połowie lat 90-tych – jedyny protokół, który Chorkendorff był w stanie odtworzyć.
Pośredniczące podejście litu do amoniaku jest obecnie jedynym, które bez cienia wątpliwości działa, zgadza się MacFarlane. Wadą litu jest to, że wiąże się on z poważną karą za wydajność energetyczną, wymagając nadpotencjału ponad 3V. 'Jest to dużo energii, która zostanie zmarnowana, utracona jako ciepło, dlatego też nie została ona podchwycona i rozwinięta wcześniej' – mówi MacFarlane.
Ale to, co protokół ma na swoją korzyść, to fakt, że zdecydowanie działa – i oferuje wiele kierunków dla przyszłych badań. Podejście oparte na działaniu litu jest naszym głównym podejściem w tej chwili,” mówi MacFarlane. Jednym z oczywistych sposobów rozwiązania problemu energetycznego jest przyjrzenie się innym metalom i ich azotkom, które przeprowadziłyby ten proces przy niższym koszcie energii, mniejszym negatywnym potencjale energetycznym', mówi.
W laboratorium Chorkendorffa nacisk kładziony jest na zrozumienie, co sprawia, że lit jest przede wszystkim skuteczny. 'Przede wszystkim zastanawiamy się, co właściwie znajduje się na tej powierzchni, aby przeprowadzić ten proces. Używamy synchrotronu w Stanford, próbując zbudować model tego procesu.'
Kilka lat temu wskaźniki były tak niskie, że nawet nie wiedzieliśmy, czy robimy amoniak
Manthiram, w międzyczasie, szukał sposobów na rozwiązanie problemu skutecznego doprowadzenia gazów do reakcji w ciekłym ogniwie elektrochemicznym. Zademonstrowaliśmy, jak można wykorzystać elektrodę dyfuzyjną do wprowadzania azotu do reaktora w sposób znacznie bardziej efektywny, przezwyciężyć ograniczenia transportowe, a tym samym wytwarzać amoniak w znacznie szybszym tempie i przy wyższej selektywności wytwarzania amoniaku w stosunku do wodoru” – mówi. Zespół osiągnął rekordową wydajność amoniaku.
Do tej pory reaktor dyfuzji gazu działa tylko przez kilka minut i przy ekstremalnym potencjale nadmiaru. 'Oni to niejako wymuszają – ale pomimo wad, bardzo podoba mi się ta praca', mówi Chorkendorff. Pokazuje on drogę naprzód i naukę, która jest potrzebna.'
Zespół – i dziedzina – ma dużo pracy, aby przekształcić proces w praktyczne rozwiązanie do nawożenia upraw lub do przechowywania i transportu energii odnawialnej, mówi Manthiram. Ale kiedy pomyślimy o tym, gdzie byliśmy w tej dziedzinie kilka lat temu, stawki były tak niskie, że nie wiedzieliśmy nawet, czy wytwarzamy amoniak. Myślę, że nasza praca pokazuje, że w końcu jesteśmy w punkcie, w którym wskaźniki są tak wysokie, że nie trzeba przeprowadzać eksperymentu kontrolnego z oznaczonym azotem, aby wykazać, że amoniak jest prawdziwy. Po prostu nie ma możliwości, aby w tych stężeniach występował przypadkowy amoniak”. Chociaż spieszy się, aby dodać, że zespół nadal robi eksperymenty kontrolne.
Na razie zespół znosi nieodłączny problem nadpotencjału litu. Jest to opłata, którą trzeba zapłacić za podążanie tą drogą, a my pogodziliśmy się z płaceniem tej ceny, ponieważ nie ma innego systemu, który może działać nawet w pobliżu szybkości, które osiągnęliśmy dzięki litowi' – mówi Manthiram. Byłbym zaskoczony, gdyby w ciągu następnej dekady nie pojawiły się inne metody, za które nie zapłacimy tej kary” – dodaje. Ale to jest to, gdzie pole jest w tej chwili.'
James Mitchell Crow jest pisarzem naukowym z Melbourne, Australia
James Mitchell Crow jest pisarzem naukowym z Melbourne, Australia
.