INTRODUCTION
La sténose valvulaire aortique est la valvulopathie acquise la plus fréquente et celle qui nécessite le plus souvent une chirurgie de remplacement valvulaire dans notre environnement.1 Pour ces patients, les évaluations par échocardiographie transthoracique (ETT) bidimensionnelle et par échocardiographie Doppler jouent un rôle important dans la détermination de la gravité de la cardiopathie valvulaire, de sa prise en charge et de son pronostic2.
Lors de l’évaluation échocardiographique, il est normal de rencontrer une aire valvulaire aortique (AVA)
cm2 avec de faibles gradients transvalvulaires malgré une fraction d’éjection préservée.3 L’impact pronostique de cette entité n’est pas bien défini. Certaines études ont suggéré que ce schéma échocardiographique est associé à un plus mauvais pronostic.4,5 Cependant, une étude prospective récente rapporte que cette entité pourrait avoir un pronostic similaire à celui de la sténose aortique, meilleur que celui rapporté précédemment, ce qui suggère une classification erronée de la gravité de la sténose de la valve aortique en utilisant les méthodes diagnostiques habituelles.6
Les techniques d’échocardiographie tridimensionnelle (3D) se sont avérées utiles pour le diagnostic de la sténose aortique7 et le suivi de son traitement.8 Il a également été démontré que l’évaluation de l’AVA par planimétrie avec l’échocardiographie transœsophagienne 3D (3D-TOE) est réalisable. Les résultats étaient cohérents avec les mesures calculées à l’aide de l’ETT.9 La planimétrie de la valve par 3D-TOE pourrait être un outil diagnostique utile pour vérifier la sévérité de la valvulopathie aortique lorsque l’étude transthoracique montre une discordance entre l’AVA estimée par l’équation de continuité et les gradients obtenus par échocardiographie Doppler.
L’objectif de cette étude était d’évaluer la concordance entre l’AVA obtenue par l’équation de continuité avec l’ETT et celle obtenue par planimétrie 3D-TOE chez des patients présentant une sténose aortique sévère et un faible gradient avec une fonction ventriculaire normale, afin d’établir l’existence de cette maladie.
METHODDesign, patients et considérations éthiques
Étude descriptive et transversale de patients consécutifs transférés dans un centre de référence entre septembre 2009 et juin 2012 pour une évaluation de la sténose aortique. Les patients présentant une sténose aortique sévère, définie par une AVA
cm2, ont été sélectionnés. Parmi cet échantillon de patients, nous avons sélectionné ceux qui présentaient un gradient aortique moyenmmHg et une fraction d’éjection ventriculaire gauche≥50%. Le protocole de l’étude a été revu et approuvé par le comité d’éthique de la recherche clinique du centre le 27 juillet 2009. Le consentement éclairé a été obtenu de tous les patients.Echocardiographie transthoracique
L’ETP a été réalisée avec un équipement d’échographie iE33 (Philips Medical Systems ; Andover, Massachusetts, États-Unis) avec une sonde sectorielle S5-2 (bande passante 5 à 1 MHZ). Des cardiologues expérimentés ont réalisé une étude standardisée en suivant les recommandations actuelles10, en utilisant toutes les vues (apicale, sous-costale, suprasternale et parasternale droite) pour obtenir une vitesse transvalvulaire maximale. Les mesures de la pression artérielle ont été enregistrées pendant l’étude. Les images obtenues ont été stockées et traitées avec un système spécialisé de gestion des images (Xcelera, Philips Medical Systems) et l’AVA a été calculée par l’équation de continuité.10 Les obstructions ventriculaires-artérielles ont été calculées selon la méthode décrite par Briand et al.11
Échocardiographie transoesophagienne tridimensionnelle
Le même jour que l’ETT standard, l’ETO a également été réalisée chez tous les patients par un échographiste en aveugle des résultats de l’étude transthoracique. La sédation au propofol était employée à la discrétion de l’échographe.
La pression sanguine était surveillée et enregistrée pendant la procédure. Le 3D-TOE a été réalisé avec un équipement d’échographie iE33 (Philips Medical Systems) avec un transducteur X7-2t. Des images en temps réel (Live 3D®) du volume pyramidal de la valve aortique et du canal de sortie du ventricule gauche (LVOT) ont été obtenues. L’angle et la profondeur de la zone explorée ont été réduits afin d’obtenir une fréquence d’acquisition supérieure à 20Hz. Les images obtenues ont été centrées sur la valve aortique à partir d’une vue en axe court entre 30° et 45°, guidée par le mode biplan (x-Plane®) de façon à obtenir l’ouverture de la valve au niveau des cuspides valvulaires (Fig. 1). Chez chaque patient, 3 cycles cardiaques ont été enregistrés.

Résultats traités avec Q-Lab® de l’imagerie de la valve aortique obtenue par la méthode Live 3D®. Les panneaux A, B et C présentent une reconstruction multiplanaire. Le panneau A contient le plan transversal au niveau des cuspides aortiques où nous avons effectué une planimétrie de la surface de la valve aortique (dans ce cas, 0,45 cm2). Le panneau B montre le plan longitudinal utilisé pour sélectionner le plan transversal au niveau des cuspides de la valve. Le panneau D montre une image tridimensionnelle d’une valve aortique bicuspide avec un raphé fibreux dans la cuspide antérieure. Sur cette image, nous avons sélectionné le cadre où l’ouverture maximale de la valve est visible.
Le post-traitement des images a été réalisé sur une station de travail Xcelera à l’aide du logiciel Q-Lab® (Philips Medical Systems). Ce logiciel de gestion d’images permet de reconstruire toute fenêtre du volume pyramidal obtenue précédemment. Sur l’image 3D, nous avons sélectionné la phase du cycle cardiaque dans laquelle l’ouverture de la valve était la plus élevée. Sur cette image, une reconstruction multiplanaire a été réalisée pour obtenir une vue perpendiculaire à la valve aortique semilunaire, réorientée si nécessaire pour visualiser la zone d’ouverture valvulaire au niveau des cuspides valvulaires (Fig. 1). De même, une planimétrie de la zone de la LVOT a été réalisée et incluse dans l’équation de continuité pour calculer l’AVA en utilisant une approche mixte : 3D-TOE pour la LVOT et TTE pour les flux.
Traitement des données et analyse statistique
Les calculs ont été effectués après 3 cycles cardiaques (5 cycles non extrêmes si le patient était en fibrillation auriculaire). Toutes les mesures et les calculs ont été effectués en aveugle et en double, par deux échocardiographistes différents.
La distribution normale des variables continues a été évaluée à l’aide du test de Kolmogorov-Smirnov (correction de Lilliefors). Les variables sont exprimées en proportions, en moyenne (écart-type) ou en médiane , selon le cas. Les comparaisons entre les estimateurs centraux ont été effectuées à l’aide du test t de Student ou du test du chi-deux. La fiabilité des mesures a été évaluée par le coefficient de corrélation intraclasse12 et le tracé de Bland-Altman.13 Le coefficient de Kappa a été utilisé pour comparer la classification de la sévérité de la sténose valvulaire par les méthodes étudiées. Les différences ont été considérées comme statistiquement significatives lorsque la valeur bilatérale était P14
RESULTATS
Entre les dates spécifiées, nous avons évalué 240 patients atteints de sténose aortique dans notre laboratoire, dont 212 avaient une AVA aortique
cm2. Parmi ces patients, 63 (29,7 %) répondaient aux critères de sténose sévère de la valve aortique avec un faible gradient et une fonction ventriculaire normale (Fig. 2). Nous n’avons pas pu réaliser de planimétrie 3D-TOE chez 2 patients en raison d’une calcification valvulaire étendue qui nous a empêchés d’identifier correctement la zone d’ouverture de la valve. Par conséquent, notre population finale était composée de 61 patients dont les caractéristiques sont présentées dans le tableau 1.
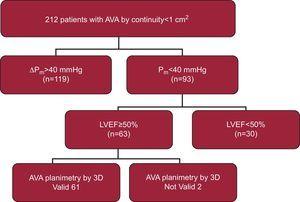
Diagramme du flux de patients. En partant de 240 patients évalués, 212 patients présentant une sténose aortique sévère ont été sélectionnés dans l’étude transthoracique. Finalement, 61 patients sont restés comme participants à notre étude. AVA, surface de la valve aortique ; FEVG, fraction d’éjection ventriculaire gauche ; ΔPm, gradient aortique moyen.
Caractéristiques des 61 patients de l’étude.
| Femme | 29 (47,5) | Age, années | 77,2±8.72 |
| BSA, m2 | 1,76±0,17 | Patients en FA | 22 (36,1) | Fréquence cardiaque, bpm | 73.6±16,6 | PES, mmHg* | 135,1±24,6 | PES, mmHg* | 71.9±12,8 | LVEF, %* | 62,82±6,98 | VTI1, cm* | 19,87±6.17 | Indice de volume systolique, mL/m2* | 32,5±9,9 |
| Gradient aortique maximal, mmHg* | 50.14±13,40 | Gradient aortique moyen, mmHg* | 29,3±7.2 | Diamètre de la LVOT, ETT, mm* | 19,4±2,3 |
| Surface de la LVOT, ETT, cm2* | 2,99±0.71 | Surface de la veine cave, 3D-TOE, cm2* | 3,40±0,97 |
| AVA, ETT, cm2* | 0.74±0,16 | AVA 3D-TOE, cm2* | 0,75±0,20 | Z, mmHg/mL/m2* | 5,40±1.83 |
3D-TOE, échocardiographie transœsophagienne tridimensionnelle ; AF, fibrillation auriculaire ; AVA, surface de la valve aortique ; BSA, surface corporelle ; DBP, pression sanguine diastolique ; LVEF, fraction d’éjection du ventricule gauche ; LVOT, voie de sortie du ventricule gauche ; SBP, pression sanguine systolique ; TTE, échocardiographie transthoracique ; VTI1 : Intégrale vitesse-temps prévalvulaire ; Z, impédance artérielle ventriculaire.
Les données sont exprimées en nombre. (%) ou moyenne±écart-type.
Mesurée pendant la 3D-TOE.
Étude de concordance
La planimétrie de l’AVA par reconstruction 3D-TOE a confirmé la présence d’une sténose sévère (AVA
cm2) dans 52 cas (85,2%). Le coefficient de corrélation intraclasse entre l’ETT et le 3D-TOE était de 0,505 (intervalle de confiance à 95 % : 0,290-0,671 ; figure 3. La différence moyenne entre les deux méthodes était de 0,003cm2, la mesure par 3D-TOE étant légèrement supérieure (IC95%, -0,353 à 0,359).
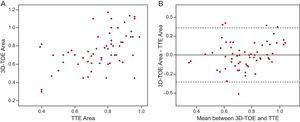
A : Dispersion graphique des mesures de la surface de la valve aortique par échocardiographie transœsophagienne tridimensionnelle et échocardiographie transthoracique. B : Graphique de Bland-Altman13 montrant la concordance des mesures de la surface de la valve aortique par échocardiographie transœsophagienne tridimensionnelle et échocardiographie transthoracique. La différence moyenne entre les 2 méthodes était y-x=0,003 (intervalle de confiance à 95 %, -0,353 à 0,359). 3D-TOE, échocardiographie transœsophagienne tridimensionnelle ; ETT, échocardiographie transthoracique.
Description du groupe mal classé
Chez 9 patients (14,7%), l’évaluation de l’AVA par TTE 3D a révélé des dimensions supérieures à 1cm2. Ces patients avaient une surface corporelle plus importante. Un seul d’entre eux présentait une fibrillation auriculaire et avait un VG et un VTG plus grands que les patients correctement classés. L’AVA par ETT était également plus grande que celle des patients correctement classés. Une comparaison des variables analysées est présentée dans le tableau 2.
Différences entre les patients selon la concordance des deux méthodes dans la classification de la sévérité aortique.
| Classification concordante (n=52). | Classification discordante (n=9) | P | |
| Age, ans | 77.9±8,5 | 73,1±8,9 | .125 |
| Homme | 23 (44,2) | 9 (100) | .001* | BSA, m2 | 1.74±0,16 | 1,90±0,18 | 0,024 | Patients en FA | 21 (40,3) | 1 (11,1) | .090* | Utilisation de sédatif | 34 (65,4) | 5 (55,5) | .138* | Tdd LV, mm | 41,9±5.4 | 51,6±9,3 |
| Tdv LV, mL | 67,4±25,5 | 103,8±36,1 | LVEF, % | 63.2±6,6 | 60,5±8,6 | .296 | LVOTD | 19,1±2,1 | 21,8±2,2 | .001 |
| SVI, mL/m2 | 31,6±9,8 | 38,3±9,8 | 0,065 | Gradient moyen, mmHg | 29,2±7.4 | 29,8±5,8 | .811 |
| AVA TTE, cm2 | 0,72±0,16 | 0,86±0,08 | .024 | AVA 3D-TOE, cm2 | 0,69±0,15 | 1,08±0,05 | Z, mmHg/mL/m2 | 5,50±1.90 | 4,46±0,63 | .194 |
3D-TOE, échocardiographie transœsophagienne tridimensionnelle ; AF, fibrillation auriculaire ; AVA, surface de la valve aortique ; BSA, surface corporelle ; LV, ventricule gauche ; LVEF, fraction d’éjection du ventricule gauche ; LVOTD, diamètre de la voie de sortie du ventricule gauche ; SVI, indice de volume systolique ; Tdd, diamètre télédiastolique ; Tdv, volume télédystolique ; TTE, échocardiographie transthoracique ; Z, impédance artérielle ventriculaire.
Les données sont exprimées en nombre. (%) ou moyenne±écart-type.
Les comparaisons ont été effectuées par des tests t de Student et le test du chi-deux.
Lorsque nous avons utilisé la zone de la LVOT obtenue par 3D-TOE dans l’équation de continuité, l’AVA obtenue était>1cm2 dans 9 cas, qui ont été reclassés comme sténose modérée. Cependant, le coefficient Kappa de concordance entre le 3D-TOE et l’évaluation par méthode mixte n’a atteint que 0,28.
Discussion
Cette étude descriptive montre que la sténose aortique sévère paradoxale à faible gradient présente chez 30 % des participants à notre étude est une entité réelle. Elle a été confirmée comme telle chez 85,2% des patients évalués par planimétrie 3D-TOE. Dans des études précédentes, la planimétrie de l’AVA à l’aide d’images 3D-TOE a également confirmé l’existence de véritables cas de sténose aortique selon les critères anatomiques.2,10
Concordance
Le coefficient de corrélation intraclasse est un outil utile pour évaluer la concordance entre différentes méthodes de mesure ou observateurs, sur la base d’un modèle d’analyse de la variance utilisant des mesures répétées.12 Dans notre étude, la concordance entre l’ETT et l’ETO 3D est modérée, avec un coefficient de corrélation intraclasse inférieur à celui rapporté précédemment dans une étude de patients atteints de sténose aortique.9 Nous attribuons ce taux de concordance plus faible à notre échantillon spécialement sélectionné. Les patients de notre étude sont ceux qui feraient douter de nombreux auteurs de la précision des mesures effectuées par l’ETT.7,15,16 L’inclusion de certains patients présentant une AVA sous-estimée par l’ETT (15% dans notre série) rend les résultats inférieurs à ceux rapportés dans une population moins sélective.9
D’autre part, nous obtenons la surface anatomique de la valve par planimétrie alors que l’équation de continuité calcule la surface valvulaire effective.7 Il a été décrit que la surface anatomique affiche des valeurs plus élevées que celles estimées par l’équation de continuité, en particulier dans les cas de valves dégénératives, plates, sans bombement, semblables à celles de la plupart de notre population d’étude.17 Nos résultats, cependant, ne montrent aucune différence significative entre les deux méthodes. Dans l’analyse du tracé de Bland-Altman, la différence moyenne des estimations était presque la même, bien que la mesure 3D-TOE soit légèrement supérieure, 0,003cm2 (95%CI, -0,353 à 0,359).
Groupe mal classé
La gravité de la valve affectée n’a pas été confirmée par la planimétrie 3D-TOE chez 9 des patients que nous avons évalués. Nous considérons qu’il s’agit d’un nombre insuffisant de cas pour établir les causes d’une mauvaise classification. Néanmoins, ces patients présentaient des mesures de surface corporelle, de LV et de LVOT plus importantes. Un seul d’entre eux présentait une fibrillation auriculaire et l’indice de volume endo-systolique était légèrement plus élevé bien qu’il n’ait pas atteint la signification statistique par rapport au groupe concordant. La plupart de ces patients présentaient une AVA par ETT>0,8cm2. Comme le montre la figure 3, un seul patient présentant une AVA de 0,75cm2 par ETT a ensuite présenté une AVA>1cm2 par 3D-TOE. Il s’agit sans aucun doute d’un groupe de patients présentant une sténose valvulaire à la limite de la sévérité.
Les erreurs potentielles dans la mesure de la LVOT sont notées dans les lignes directrices pour la quantification de la valvulopathie10 et sont soupçonnées d’être responsables d’une mauvaise classification dans certaines études6. Étant donné que la morphologie de la LVOT n’est pas circulaire, l’utilisation d’autres méthodes telles que l’estimation de la surface de la LVOT par 3D-TOE a été encouragée pour améliorer la fiabilité de la mesure7 et aider à éviter les résultats insatisfaisants du traitement.18 Dans notre étude, l’utilisation de la surface de la LVOT évaluée par 3D-TOE nous a permis de reclasser certains patients au niveau modéré qui avaient une AVA>1cm2. Cependant, des patients ont également été mal classés en utilisant les résultats de la 3D-TOE, de sorte que le coefficient Kappa n’était pas très bon (0,28).
En raison de la conception des critères d’inclusion, le groupe de patients mal classés ne peut rendre compte que des cas dans lesquels le degré de gravité de la sténose aortique diminue. Par conséquent, tirer des conclusions de ce groupe serait très sensible au phénomène de régression vers la moyenne,19 comme nous l’avons reconnu.
Limitations
Cette étude ne dispose pas d’un critère de référence pour l’estimation de l’AVA. La norme clinique est l’ETT avec l’équation de continuité2,10 mais le phénomène d’incohérence de cette méthode3 est précisément ce que nous avons cherché à étudier. Nous avons opté pour une méthodologie réalisable qui quantifie l’AVA en utilisant une stratégie de mesures indépendantes du Doppler et du LVOT. Cependant, le 3D-TOE présente d’importantes limitations, notamment au niveau de sa résolution spatiale et temporelle. Avec une fréquence d’acquisition de 20Hz et une fréquence cardiaque d’environ 70 bpm, elle peut obtenir entre 6 et 7 images pendant la systole cardiaque. En général, c’est à la 5ème ou 6ème image que l’on capture l’ouverture valvulaire maximale. Il est également possible, dans certains cas, de ne pas obtenir l’image d’ouverture valvulaire maximale.
La sédation au propofol nous permet d’explorer en profondeur et permet au patient d’être plus confortable. Bien que les effets du propofol sur la contractilité et la tension artérielle aient été mentionnés,20 ils ne semblent pas avoir influencé nos résultats car lorsque les patients de l’un ou l’autre groupe ont été reclassés, il n’y avait pas de différences liées à son utilisation. De plus, nous considérons que le contrôle de la fréquence cardiaque et la possibilité d’un examen approfondi sont d’une grande importance ; par conséquent, en cas de doute, nous préférons l’aide apportée par le sédatif.
Chez certains patients, la présence de calcifications étendues, en particulier celles situées à la face arrière de la racine ou sur la cuspide postérieure, nous empêche d’évaluer l’ouverture. Cela ne s’est produit que chez deux patients.
Bien que l’inclusion des patients ait été consécutive, un biais d’orientation est possible car nous n’avons inclus que des patients présentant une sténose sévère antérieure. Cela signifie que l’échantillon peut ne pas représenter la population générale. Les différents critères d’inclusion utilisés par différents auteurs peuvent expliquer les différences de prévalence de la sténose sévère à faible gradient paradoxal rapportées dans la littérature.
CONCLUSIONS
La sténose aortique sévère malgré un faible gradient paradoxal est une entité réelle confirmée dans 85% des cas évalués par 3D-TOE. Une étude plus approfondie des cas présentant des divergences est nécessaire pour découvrir les raisons de leur mauvaise classification.
CONFLICTS D’INTÉRÊT
Aucun n’a été déclaré.