Introduction
ニューロンは、周囲の何千もの他のニューロンから絶えず入力を受けています。 しかし、これらの入力が活動電位を引き起こすことができるかどうかは、これらの入力の和に依存します。 興奮性の信号と抑制性の信号が一緒になって、活動電位を発生させることができるかどうかのプロセスと定義することができます。

和算には2つのタイプがあり、それぞれ時間和と空間和と呼ばれます。 空間的な和は、複数の同時入力からの信号と定義することができます。 一方、時間的和は、繰り返し入力された信号です。 基本的に活動電位を得るためには、閾値電圧に到達する必要があります。
シナプス前の神経細胞から放出される神経伝達物質には2つのタイプがあります。
シナプス前の神経細胞から放出される神経伝達物質には2種類あり、興奮性の神経伝達物質では脱分極が起こり、これを興奮性シナプス後電位(EPSP)と呼びます。 抑制性の神経伝達物質によって過分極が起こり、これを抑制性シナプス後電位(IPSP)と言います。 神経細胞は、様々な方法で互いに影響を与えることができます。
脱抑制は、神経伝達物質が過分極を起こし、抑制性シナプス後電位(IPSP)を発生させます。
脱抑制とは、経路を容易にする興奮性入力を取り除くことです。
ニューロン上の複数のソース入力は、空間的に合計することができますが、初期の入力が減衰しないように、入力の間隔を密にする必要があります。
ニューロン上の複数のソース入力は、空間的に合計することができますが、初期の入力が減衰しないように、密接な間隔で入力を行う必要があります。
しきい値に達して活動電位が発生するかどうかを決定するもう一つの重要な要因は、シナプスと神経細胞体の間の距離です。 シナプスと細胞体の距離が近ければ近いほど、総和が大きくなり、活動電位が誘発されやすくなります。
シナプス後の神経細胞の移動手段は、ご存知のように樹状突起です。 この樹状突起には、電圧ゲート式のイオンチャネルがほとんどありません。
シナプス後細胞の移動手段は樹状突起です。 この神経細胞体は、これらの入力電位を合計します。
空間的和算
複数のニューロンからの入力が活動電位を引き起こす場合、これは空間的和算と呼ばれます。 これらの電位は主に樹状突起からのもので、これらの入力を加算して空間的和を得ます。
興奮性シナプス後電位の数が多いほど、その電位が活動電位を誘発する閾値に達する可能性が高くなります。 同様に、抑制性シナプス後電位の数が多ければ多いほど、活動電位を発生させるための閾値電位に到達する可能性は低くなります。
活動電位が発生する可能性は、樹状突起の入力が軸索のヒロックにどれだけ近いかにも大きく影響されます。
活動電位が発生する可能性は、樹状突起の入力が軸索の丘にどれだけ近いかにも大きく影響されます。
Temporal Summation
大量のシナプス前神経細胞の活動電位がシナプス後神経細胞の活動電位を誘発し、それが互いに合流することをTemporal Summation(時間的合流)といいます。
この場合、活動電位の間隔はシナプス後の活動電位の持続時間よりも短くなります。
この場合、活動電位の間隔はシナプス後の活動電位の持続時間より短くなります。
仕組み
シナプス後細胞にはイオンチャネルがあり、神経伝達物質が受容体に結合するとイオンチャネルが開いたり閉じたりします。 これらのチャネルの開閉により、シナプス後電位が発生します。 シナプス後電位には2つのタイプがあります。 興奮性シナプス後電位は、活動電位を開始する可能性を高めるものです。
興奮性神経伝達物質(グルタミン酸)
興奮性神経伝達物質の代表的なものにグルタミン酸があります。 このグルタミン酸は、シナプス後膜のAMPA受容体に結合します。 この結合により、ナトリウムのカチオンが流入します。 このナトリウムの流入により、脱分極が起こります。 これをEPSP(Excitatory Postynaptic Potential)といいます。 EPSPが閾値に達するためには、これらの入力が多数必要であることに注意する必要があります。 神経伝達物質の効果は、シナプス前のインパルスよりもはるかに長く続きます。
興奮性シナプス後電位と活動電位の違いは、興奮性シナプス後電位がその入力を合計することができ、活動電位を刺激して閾値に到達するか、まったく到達しないかのオール・オア・ナッシングの反応とは対照的に、段階的な反応を作り出すことです。
抑制性神経伝達物質(GABA)
GABAは抑制性シナプス後電位(IPSP)に関与する主な神経伝達物質です。 GABAは、シナプス後の神経細胞の受容体に結合すると、グルタミン酸などの興奮性神経伝達物質によるEPSPとは異なる特定のイオンチャネルを開きます。 これらのチャネルは負電荷の陰イオンの流入と正電荷の陽イオンの流出を可能にします。 このケースでは、陰イオンは塩化物イオンです。 流れ出た陽イオンはカリウムイオンです。 どちらのイオンも同じように膜電位を下げ、シナプス後の神経細胞を過分極させます。
これらのIPSPと膜電圧の低下が重なると、しきい値電位から外れて活動電位が抑制されます。 しかし、これらのIPSPsとEPSPsは同時に起こっている可能性があり、シナプス後のニューロンはグルタミン酸からの興奮性シグナルとGABAからの抑制性シグナルを受け取っている可能性があります。 抑制性グルタミン酸の目的は、過分極によって膜電位を閾値から遠ざけることです。
EPSPとIPSPの代数的処理
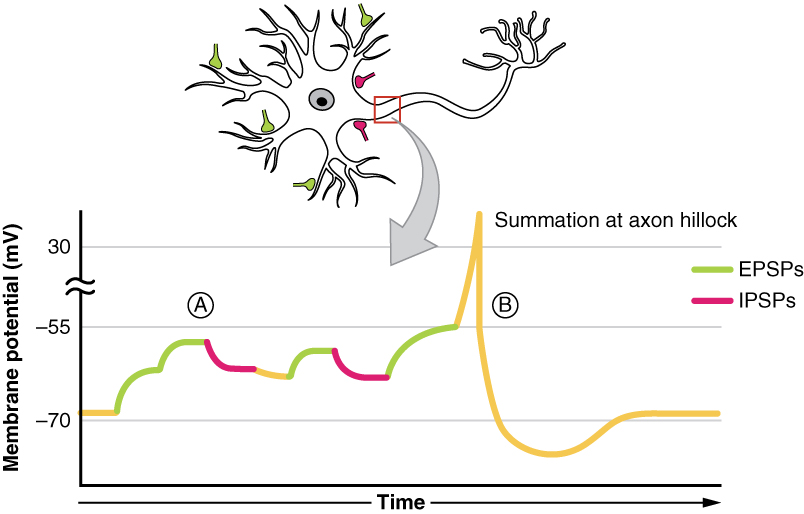
どの時点のニューロンでも、多数のEPSPとIPSPの入力を同時に受けているはずです。 閾値電位に達して活動電位が誘発されるかどうかの出力を決定するためには、これらのEPSPとIPSPの代数的な処理を行う必要があります。
この出力は、ナトリウムイオンチャネルを介してナトリウムイオンを流入させるグルタミン酸のような興奮性神経伝達物質や、塩化物イオンチャネルやカリウムイオンチャネルを介して塩化物イオンやカリウムイオンを流入させるGABAのような抑制性神経伝達物質など、それぞれの種類の神経伝達物質の数に依存しています。 このシナプスは、これらのIPSPsとEPSPsの代数的な処理によって出力が決定される決定点と呼ぶことができます。
軸索ヒロック

ニューロンの細胞体のうち、軸索に接続する部分を軸索ヒロックと呼びます。 そこにはニッスル物質がまばらに分布しています。 これは、光学顕微鏡で確認することができます。 この軸索丘部は、ニューロンの軸索と体幹をつなぐため、シナプスからの入力による膜電位の総和が起こる体幹の最終領域である。
この軸索丘は、ニューロンの体細胞と軸索をつなぐ部分で、シナプスからの入力による膜電位の和が体細胞の最後の領域で起こり、この和が軸索に伝えられる。
過去には、軸索の丘が活動電位が開始されるトリガーゾーンであると多くの人が考えていましたが、現在では、最初の無髄軸索のセグメントと軸索の丘のピークの間の最初のセグメントが活動電位が開始される場所であると考えられています。 活動電位が開始される軸索の正点は、細胞ごとに異なります。
ホルモンの刺激や神経伝達物質のセカンドメッセンジャー効果によっても、この正位置が変わることがあります。
膜電位を細胞の体部または軸索部に局在化させるには、軸索と細胞体の間に明確な膜ドメインを画定する必要があります。
シャント
ニューロンでは、樹状突起の興奮性シナプス後電位と抑制性シナプス後電位が互いに非常に接近していることがよくあります。 これを「シャント」といいます。 また、樹状突起だけでなく、細胞の体部でもシャントが起こることがあります。
時間的には、これらの興奮性シナプス後電位と抑制性シナプス後電位を合計して、その結果、閾値に達して活動電位が発生するかどうかの出力を決定することになります。 しかし、この一連のイベントがコールの体細胞で起こった場合、抑制性入力によって細胞の抵抗が変化します。 細胞は漏出し始め、これにより、興奮性入力の影響を取り除くのとは対照的に、シャントが形成されます。
治療への応用
侵害刺激について議論するとき、時間的総括は反復的な痛みの刺激の統合です。 一方、空間的総括とは、広い範囲からの侵害受容性入力の統合である。 多くの慢性疾患では、痛みの持続時間が長く、しかも広範囲に及ぶという症状があります。 そのため、慢性疾患では、時間的および空間的な侵害受容性の和が見られます。 圧力刺激の実験は、侵害受容入力の時間的な和が、空間的な和によって促進されるという事実を証明しています。
研究
空間的和のほとんどの実験は、光ニューロンと感覚ニューロンでテストされていますが、これは興奮性ニューロンと抑制性ニューロンの周波数が一定の範囲であるためです。 最近の研究では、ニューロンの細胞体や樹状突起のシナプス後電位の減衰が神経和合の大きな焦点となっています。 これらの相互作用の応答は、個々の応答の合計よりも小さいという事実から、これらの応答は非線形と表現されます。 この効果をもたらす一般的な原因としてShuntingがあります。 シャントとは、興奮性シナプス後電位のコンダクタンスが減少することです。
越後直樹氏とマイケル・アリエル氏は、カメの基底部視床核で実験を行い、シャント抑制に関する情報を得ることができました。 彼らの研究によると、EPSPとIPSPの空間的な和により、抑制性反応の間に興奮性反応が減衰することがわかりました。 また、減衰後には興奮性反応の増大が見られたという。 この実験のコントロールは、過分極電流がこれらの電圧感受性チャンネルを活性化するときの減衰をテストすることであった。 その結果、減衰は過分極ではなく、シナプス受容体チャネルの開口部によって引き起こされると結論づけられました。
結論
ある時点で、ニューロンは複数の異なるニューロンから複数の入力を受け取っています。
これらの入力には、興奮性のものと抑制性のものがありますが、しきい値電位に達して活動電位が誘発されるかどうかを決定するためには、いくつかの要因を考慮する必要があります。
神経伝達物質によって作用が異なります。グルタミン酸などの興奮性神経伝達物質は、ナトリウムイオンチャネルを開き、ナトリウムイオンを流入させて膜電位を上昇させます。 また、GABAのような抑制性の神経伝達物質は、塩化物イオンチャネルを開いて塩化物イオンを流入させたり、カリウムイオンチャネルを開いてカリウムイオンを流出させたりします。
この2つの作用により、膜電位は低下し、閾値電圧から外れて活動電位が発生する可能性が低くなります。
活動電位が発生する可能性を高めるもう一つの要因は、樹状突起の入力が軸索の丘にどれだけ近いかということです。
興奮状態にあるニューロンは、軸索に接続された体細胞の一部である軸索丘と呼ばれます。
興奮性の神経伝達物質は脱分極の可能性を高め、膜電圧の変化は興奮性シナプス後電位(EPSP)と呼ばれます。 抑制性の神経伝達物質は過分極の可能性を高め、この膜電位の変化は抑制性シナプス後電位(IPSP)と呼ばれます。
しきい値電圧に達して活動電位が発生するかどうかは、個々の入力の代数的な総和によって決まります。 和算には2つのタイプがあります。
活動電位を引き起こす複数の異なるシナプス前ニューロンからの複数の入力の総和は、空間的総和と呼ばれます。
1つのシナプス前ニューロンからの高頻度の入力をまとめて活動電位を発生させることを時間的加算といいます。 このシナプス後電位の持続時間は、それぞれの活動電位間の持続時間よりも長くなります
。