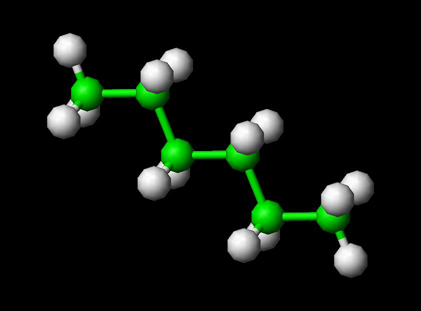
Para ver a Hexane Molecule em 3D —>>em 3D com Jsmol
Propriedades Químicas e Físicas da Molécula Hexano
Hexano é um hidrocarboneto alcano com a fórmula química CH3(CH2)4CH3. O prefixo “hex” refere-se aos seus seis carbonos, enquanto que o final “ane” indica que os seus carbonos estão ligados por ligações simples. Os isómeros hexanos são em grande parte não reactivos, e são frequentemente utilizados como solvente inerte em reacções orgânicas, porque são muito não polares. São também constituintes comuns da gasolina e colas utilizadas para calçado, produtos de couro e telhados. Além disso, são utilizados em solventes para extrair óleos para cozinhar e como agente de limpeza para calçado, mobiliário e fabrico têxtil.
Produção
Hexano é produzido pela refinação de petróleo bruto. A composição exacta da fracção depende em grande parte da fonte do óleo (bruto ou reformado) e das restrições da refinação. O produto industrial (normalmente cerca de 50% em peso do isómero de cadeia recta) é a fracção a ferver a 65-70 °C.
Toxicidade
A toxicidade aguda do hexano é relativamente baixa, embora se trate de um anestésico suave. A inalação de altas concentrações produz primeiro um estado de euforia suave, seguido de sonolência com dores de cabeça e náuseas.
Intoxicação crónica por hexano tem sido observada em abusadores de solventes recreativos e em trabalhadores nas indústrias de fabrico de calçado, restauração de mobiliário e construção automóvel. Os sintomas iniciais são formigueiro e cãibras nos braços e pernas, seguidos de fraqueza muscular geral. Em casos graves, observa-se atrofia dos músculos esqueléticos, juntamente com uma perda de coordenação e problemas de visão.
Similares sintomas são observados em modelos animais. Estão associados a uma degeneração do sistema nervoso periférico (e eventualmente do sistema nervoso central), começando com as porções distais dos axónios nervosos mais longos e mais largos. A toxicidade não se deve ao hexano em si, mas a um dos seus metabolitos, o hexano-2,5-diona. Acredita-se que isto reage com o grupo amino da cadeia lateral dos resíduos de lisina nas proteínas, causando uma ligação cruzada e uma perda da função proteica.
Os efeitos do envenenamento por hexano nos humanos são incertos. Em 1994, o n-hexano foi incluído na lista de produtos químicos do Toxic Release Inventory (TRI). Na última parte do século XX e início do século XXI, foram atribuídas várias explosões à combustão do gás hexano. Em 2001, a Agência de Protecção Ambiental dos EUA emitiu regulamentos sobre o controlo das emissões de gás hexano devido às suas potenciais propriedades cancerígenas e preocupações ambientais.
Usos
Na indústria, os hexanos são utilizados na formulação de colas para calçado, produtos de couro, e telhados. São também utilizados para extrair óleos alimentares (tais como óleo de canola ou óleo de soja) de sementes, para limpeza e desengorduramento de uma variedade de artigos, e no fabrico de têxteis. É comummente utilizado na extracção de óleo de soja à base de alimentos nos Estados Unidos, e é um contaminante potencialmente presente em todos os produtos alimentares de soja utilizando a técnica, que é controversa e não regulamentada pela FDA.
Um uso típico de laboratório de hexanos é a extracção de óleo e gorduras contaminantes da água e do solo para análise. Uma vez que o hexano não pode ser facilmente desprotegido, é utilizado em laboratório para reacções que envolvem bases muito fortes, tais como a preparação de organolídios. Por exemplo, os butilithiums são normalmente fornecidos como uma solução de hexano.
Hexanos são normalmente utilizados em cromatografia como solvente não polar. Os alcanos superiores presentes como impurezas nos hexanos têm tempos de retenção semelhantes aos do solvente, o que significa que as fracções contendo hexano também conterão estas impurezas. Na cromatografia preparatória, a concentração de um grande volume de hexanos pode resultar numa amostra que está sensivelmente contaminada por alcanos. Isto pode resultar na obtenção de um composto sólido como óleo e os alcanos podem interferir na análise.
Em muitas aplicações (especialmente farmacêuticas), a utilização do n-hexano está a ser gradualmente eliminada devido à sua toxicidade a longo prazo. É frequentemente substituído por n-heptano, que não irá formar o metabolito tóxico hexano-2,5-diona.