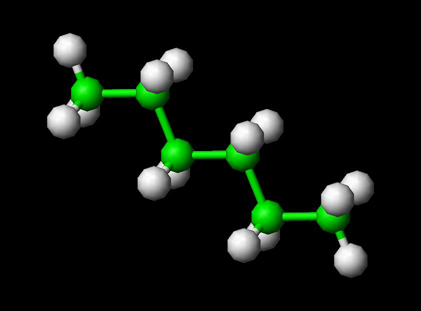
Para ver la molécula de hexano en 3D —>>en 3D con Jsmol
Propiedades químicas y físicas de la molécula de hexano
El hexano es un hidrocarburo alcano con la fórmula química CH3(CH2)4CH3. El prefijo «hex» se refiere a sus seis carbonos, mientras que la terminación «ane» indica que sus carbonos están conectados por enlaces simples. Los isómeros del hexano son poco reactivos y se utilizan con frecuencia como disolventes inertes en reacciones orgánicas porque son muy apolares. También son componentes comunes de la gasolina y de las colas utilizadas para el calzado, los productos de cuero y los tejados. Además, se utiliza en disolventes para extraer aceites para cocinar y como agente limpiador para la fabricación de calzado, muebles y textiles.
Producción
El hexano se produce mediante el refinado del petróleo crudo. La composición exacta de la fracción depende en gran medida del origen del petróleo (crudo o reformado) y de las limitaciones del refinado. El producto industrial (normalmente alrededor del 50% en peso del isómero de cadena recta) es la fracción que hierve a 65-70 °C.
Toxicidad
La toxicidad aguda del hexano es relativamente baja, aunque es un anestésico suave. La inhalación de altas concentraciones produce primero un estado de euforia leve, seguido de somnolencia con dolores de cabeza y náuseas.
Se ha observado una intoxicación crónica por hexano en personas que abusan de los disolventes de forma recreativa y en trabajadores de las industrias de fabricación de calzado, restauración de muebles y construcción de automóviles. Los síntomas iniciales son hormigueos y calambres en brazos y piernas, seguidos de debilidad muscular general. En los casos graves, se observa atrofia de los músculos esqueléticos, junto con una pérdida de coordinación y problemas de visión.
Se observan síntomas similares en modelos animales. Se asocian a una degeneración del sistema nervioso periférico (y eventualmente del sistema nervioso central), empezando por las porciones distales de los axones nerviosos más largos y anchos. La toxicidad no se debe al hexano en sí, sino a uno de sus metabolitos, el hexano-2,5-diona. Se cree que éste reacciona con el grupo amino de la cadena lateral de los residuos de lisina en las proteínas, provocando la reticulación y la pérdida de la función proteica.
Los efectos de la intoxicación por hexano en los seres humanos son inciertos. En 1994, el n-hexano se incluyó en la lista de sustancias químicas del Inventario de Emisiones Tóxicas (TRI).A finales del siglo XX y principios del XXI, se han atribuido varias explosiones a la combustión de gas hexano. En 2001, la Agencia de Protección Medioambiental de Estados Unidos emitió una normativa sobre el control de las emisiones de gas hexano debido a sus potenciales propiedades cancerígenas y a la preocupación por el medio ambiente.
Usos
En la industria, los hexanos se utilizan en la formulación de pegamentos para zapatos, productos de cuero y techos. También se utilizan para extraer aceites de cocina (como el de canola o el de soja) de las semillas, para limpiar y desengrasar una gran variedad de artículos, y en la fabricación de textiles. Se utiliza habitualmente en la extracción de aceite de soja a partir de alimentos en los Estados Unidos, y es un contaminante potencialmente presente en todos los productos alimenticios de soja que utilizan la técnica, que no está regulada por la FDA de forma controvertida.
Un uso típico de los hexanos en el laboratorio es la extracción de contaminantes de aceite y grasa del agua y del suelo para su análisis. Dado que el hexano no puede desprotonarse fácilmente, se utiliza en el laboratorio para reacciones que implican bases muy fuertes, como la preparación de organolitos. Por ejemplo, los butilitios suelen suministrarse como solución de hexano.
Los hexanos se utilizan habitualmente en cromatografía como disolvente no polar. Los alcanos superiores presentes como impurezas en los hexanos tienen tiempos de retención similares a los del disolvente, lo que significa que las fracciones que contienen hexano también contendrán estas impurezas. En la cromatografía preparatoria, la concentración de un gran volumen de hexanos puede dar lugar a una muestra sensiblemente contaminada por alcanos. Esto puede dar lugar a que se obtenga un compuesto sólido en forma de aceite y los alcanos pueden interferir en el análisis.
En muchas aplicaciones (especialmente farmacéuticas), el uso del n-hexano se está eliminando progresivamente debido a su toxicidad a largo plazo. A menudo se sustituye por el n-heptano, que no forma el metabolito tóxico hexano-2,5-diona.