La N-Bromosuccinimida (NBS) es un agente bromante y oxidante que se utiliza como fuente de bromo en reacciones radicales (por ejemplo: bromaciones alílicas) y diversas adiciones electrofílicas. La bromación con NBS de sustratos como alcoholes y aminas, seguida de la eliminación del HBr en presencia de una base, conduce a los productos de oxidación neta en los que no se ha incorporado bromo.
Nombre de las reacciones
Reacción de Wohl-Ziegler
Literatura reciente

Se ha desarrollado un procedimiento eficaz y de fácil manejo para laSe ha desarrollado un procedimiento eficiente y fácil de usar para la desprotección oxidativa de éteres de tetrahidropiranilo (THP) con N-bromosuccinimida (NBS) utilizando β-ciclodextrina (β-CD) en agua. Una serie de éteres de tetrahidropiranilo fueron desprotegidos oxidativamente a temperatura ambiente en rendimientos impresionantes.
M. Narender, M. S. Reddy, K. R. Rao, Synthesis, 2004,1741-1743.

Las N-alcoxiamidas dan lugar convenientemente a los correspondientes ésteres carboxílicos en presencia de NBS en tolueno a través del homocoupling oxidativo y la posterior desnitrogenación térmica. Incluso los sustratos que llevan un sustituyente voluminoso o de cadena larga dieron productos en buenos rendimientos en este enfoque conveniente y económico para una transformación directa de una fracción de alcoxiamida en el grupo funcional éster carboxílico.
N. Zhang, R. Yang, D. Zhang-Negrerie, Y. Du, K. Zhao, J. Org. Chem, 2013,78, 8705-8711.

Transformación directa de etilarenos en amidas aromáticas primarias con N-bromosuccinimida y NH3 acuoso
S. Shimokawa, Y. Kawagoe, K. Moriyama, H. Togo, Org. Lett, 2016, 18, 784-787.

Una reacción eficiente, libre de metales y bases, quimioselectiva de ácidos borónicos con radicales cianamidilo/arilcianamidilo proporciona aril-, heteroarilo- y alquil aminas primarias a temperatura ambiente en 1 h. La reacción está mediada por PIFA y NBS.
N. Chatterjee, M. Arfeen, P. V. Bharatam, A. Goswami, J. Org. Chem, 2016,81, 5120-5127.
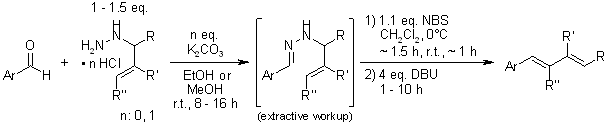
Una síntesis estereoselectiva de dienos a partir de aldehídos y derivados de N-alilhidrazina ofrece altos niveles de (E)-estereoselectividad para una variedad de sustratos. La adición de un dienófilo a la mezcla de reacción permite una secuencia de síntesis-cicloadición de dienos en un solo frasco.
D. A. Mundal, K. E. Lutz, R. J. Thomson, Org. Lett., 2009,11, 465-468.

Se consigue una transformación eficiente en un solo paso de compuestos β-hidroxicarbonílicos a compuestos α-bromados de 1,3dicarbonilo con MoO2Cl2 en presencia de N-bromosuccinimida. Todas las reacciones se llevaron a cabo en condiciones suaves y proporcionan buenos rendimientos. No se produce bromación en las posiciones bencílica y alílica.
K. Jeyakumar, D. K. Chand, Synthesis, 2009, 306-310.

K. Jeyakumar, D. K. Chand, Synthesis, 2009, 306-310.

Se lograron oxihalogenaciones selectivas de alquinos en agua bajo condiciones muy suaves en presencia de reactivos halogenantes baratos, como N-bromosuccinimida y N-clorosuccinimida, y FI-750-M como anfifilo. No se detectó ninguna halogenación en los anillos aromáticos. El medio de reacción y el catalizador pueden reciclarse.
L. Finck, J. Brals, B. Pavuluri, F. Gallou, S. Handa, J. Org. Chem., 2018, 83, 7366-7372.

Una halogenación reductora catalizada por óxido de trifenilfosfina de una cetona α,β-insaturada con triclorosilano como reactivo reductor y una N-halosuccinimida como fuente de halógeno electrofílica permite una síntesis selectiva de α-halocetonas asimétricas.
Z. Lao, H. Zhang, P. H. Toy, Org. Lett., 2019, 21, 8149-8152.

Las reacciones de hidroaluminación α-selectiva, fiables y operacionalmente sencillas, proceden en presencia de hidruro de diisobutilaluminio y (Ni(dppp)Cl2) y, a diferencia de las transformaciones no catalizadas, generan pocos o ningún subproducto de alquilaluminio. Los haluros de α-vinilo y boronatos derivados pueden sintetizarse mediante tratamiento directo con los electrófilos adecuados.
F. Gao, A. H. Hoveyda, J. Am. Chem. Soc., 2010, 132, 10961-10963.

La captura de una especie diazo de forma intermolecular por dos especies de iones independientes en tándem en el centro del carbeno instala un electrófilo y un nucleófilo en el mismo carbono. Este concepto sin metales permite la síntesis regioselectiva de varios haluros de vinilo, sulfonas de vinilo y derivados de alquinos.
D. P. Ojha, K. R. Prabhu, Org. Lett., 2015,17, 18-21.

Los compuestos no saturados como alquenos, alquinos, alenos y metilenciclopropanos (MCP) pueden ser dibromados en cuestión de minutos por NBS y bromuro de litio en THF a temperatura ambiente en rendimientos buenos a excelentes en condiciones suaves.
L.-X. Shao, M. Shi, Synlett, 2006, 1269-1271.

L.-X. Shao, M. Shi, Synlett, 2006, 1269-1271.

L.-X. Shao, M. Shi, Synlett, 2006, 1269-1271.

El uso de la N-bromosuccinimida permite una estrategia de un solo paso libre de metales para la síntesis de α-amino cetonas de importancia farmacéutica a partir de alcoholes secundarios benzílicos y aminas fácilmente disponibles. Esta reacción procede a través de tres pasos consecutivos que implican la oxidación de los alcoholes, la α-bromación de las cetonas y la sustitución nucleofílica de las α-bromo-cetonas para dar α-amino-cetonas.
S. Guha, V. Rajeshkumar, S. S. Kotha, G. Sekar, Org. Lett., 2015,17, 406-409.

Una combinación de N-bromoimida y DBU permite reacciones de aminación alílica de alquenos, en las que se pueden instalar directamente nucleófilos de nitrógeno tanto internos como externos. La doble activación de NBS o NBP por DBU da lugar a más bromo electrofílico y más átomos de nitrógeno nucleofílicos simultáneamente. Este protocolo proporciona un acceso complementario a la aminación alílica en condiciones suaves.
Y. Wei, F. Liang, X. Zhang, Org. Lett., 2013,15, 5186-5189.

Se reporta un método conveniente y eficiente para la aminobromación de alquilidenciclopropanos. Esto se ejemplifica en la preparación estereoselectiva de N–p-toluenesulfonamidas utilizando p-toluenesulfonamida y N-bromosuccinimida (NBS) como fuentes de nitrógeno y bromo, respectivamente.
X. Huang, W.-J. Fu, Synthesis, 2006, 1016-1017.

En un protocolo de flujo continuo para la bromación de compuestos benzílicos con sólo un pequeño exceso de N-bromosuccinimida, las reacciones radicales se activaron con una lámpara fluorescente compacta (CFL) de uso doméstico fácilmente disponible utilizando un diseño de reactor de flujo simple basado en tubos de polímero de etileno fluorado transparente. Todas las reacciones se llevaron a cabo utilizando acetonitrilo como disolvente, evitando así los peligrosos disolventes clorados como el CCl4.
D. Cantillo, O. de Frutos, J. A. Rincón, C. Mateos, C. O. Kappe, J. Org. Chem., 2014,79, 223-229.

La base de Lewis Trip-SMe (Trip = triptycenyl) cataliza una halogenación electrofílica de compuestos aromáticos no activados utilizando N-halosuccinimidas (NXS) a temperatura ambiente en presencia de AgSBF6 como fuente de un anión no coordinador. El sistema π de la funcionalidad del triptycenilo ejerce un papel crucial para la mejora de la electrofilia.
Y. Nishii, M. Ikeda, Y. Hayashi, S. Kawauchi, M. Miura, J. Am. Chem. Soc., 2020, 142, 1621-1629.

Se ha logrado una bromación altamente regioselectiva de compuestos aromáticos activados utilizando N-bromosuccinimida en bromuro de tetrabutilamonio. La monobromación predominantemente para-selectiva de los aromáticos activados, la aceleración de la velocidad para los sustratos menos reactivos en la adición de arcilla de montmorillonita K-10 ácida, con o sin asistencia de microondas, son las características notables de este protocolo.
N. C. Ganguly, P. De. S. Dutta, Synthesis, 2005, 1103-1108.

El uso de un hexafluoroisopropanol como disolvente permite una halogenación suave y regioselectiva de una amplia gama de arenos y heterociclos con N-halosuccinimidas en buenos rendimientos. Además, la versatilidad del método se demuestra mediante el desarrollo de reacciones de dihalogenación secuencial de una sola vez y de acoplamiento cruzado halogenación-Suzuki.
R.-J. Tang, T. Milcent, B. Crousse, J. Org. Chem., 2018, 83, 930-938.

Una halogenación altamente paraselectiva de arenos que llevan grupos coordinadores de electrones en presencia de una sal de dimidazolio rpovide p-haloarenos en buenos rendimientos. Se propone un mecanismo plausible para la reacción catalítica.
J. Chen, X. Xiong, Z. Chen, J. Huang, Synlett, 2015, 26, 2831-2834.

Los compuestos aromáticos altamente desactivados se monobromaron sin problemas mediante el tratamiento con N-bromosuccinimida (NBS) en ácido sulfúrico concentrado. Las condiciones de reacción suaves y la sencilla preparación proporcionan una ruta práctica y comercialmente viable para la síntesis de compuestos bromados de aromáticos desactivados en buenos rendimientos.
K. Rajesh, M. Somasundaram, R. Saiganesh, K. K. Balasubramanian, J. Org. Chem., 2007,72, 5867-5869.

Las n-halosuccinimidas se activan eficientemente en ácido trifluorometanosulfónico y BF3-H2O, permitiendo las halogenaciones de los aromáticos desactivados. El BF3-H2O es más económico, fácil de preparar, no se oxida y ofrece una acidez suficientemente alta.
G. K. S. Prakash, T. Mathew, D. Hoole, P. M. Esteves, Q. Wang, G. Rasul, G. A. Olah, J. Am. Chem. Soc., 2004,126, 15770-15776.

Los ácidos borónicos ariales y heteroarilicos reaccionan con N-iodosuccinimida y N-bromosuccinimida para dar los correspondientes yodo- y bromo-arenos en rendimientos buenos a excelentes. La reacción suele ser altamente regioselectiva y sólo da el producto ipso-sustituido.
C. Thiebes, G. K. Surya Prakash, N. A. Petasis, G. A. Olah, Synlett, 1998, 141-142.

Una reacción de ortobromación y yodación de alto rendimiento, general y práctica de diferentes clases de compuestos aromáticos se produce mediante la metodología de activación de enlaces C-H catalizada por Rh(III)
N. Schröder, J. Wencel-Delord, F. Glorius, J. Am. Chem. Soc., 2012, 134, 8298-8301.

Usando ciano como grupo director, una reacción de ortohalogenación (I, Br, Cl) catalizada por paladio dio rendimientos de buenos a excelentes. El método es compatible con los arilnitrilos con grupos que retiran o donan electrones. El presente método se aplicó con éxito a la síntesis de los precursores de paucifloral F e isopaucifloral F.
B. Du, X. Jiang, P. Sun, J. Org. Chem., 2013,78, 2786-2791.

Un protocolo eficiente para una síntesis altamente estereoselectiva en un solo paso de yoduros de vinilo (E)-β-arilo y bromuros de vinilo (E)-β-arilo a partir de estirenos se basa en un acoplamiento siliativo catalizado por rutenio seguido de una reacción de halodesilación mediada por N-halosuccinimida.
P. Pawluć, G. Hreczycho, J. Szudkowska, M. Kubicki, B. Marciniec, Org. Lett., 2009,11, 3390-3393.

Usando trietilamina como catalizador en reacciones de Hunsdiecker con N-halosuccinimidas como fuente de Br+ o I+, los ácidos cinámicos y los ácidos propiólicos se convierten en los correspondientes α-halostirenos y 1-halo-1-alquinos en buenos rendimientos aislados en 1-5 min.
J. Prakash, S. Roy, J. Org. Chem., 2002, 67, 7861-7864.

J. Prakash, S. Roy, J. Org. Chem., 2002, 67, 7861-7864.

Los bromuros de (E)-β-arilvinilo se prepararon fácilmente en un tiempo de reacción corto (1-2 min) mediante la irradiación por microondas de los correspondientes ácidos3-arilpropenoicos en presencia de N-bromosuccinimida y una cantidad acatalítica de acetato de litio.
C. Kuang, Q. Yang, H. Senboku, M. Tokuda, Synthesis, 2005,1319-1325.

Una síntesis eficiente de α-iodo/bromo-α,β-aldehídos/cetonas insaturados directamente a partir de alcoholes propargílicos es catalizada de forma colaborativa por Ph3PAuNTf2 y MoO2(acac)2, y Ph3PO como aditivo ayuda a suprimir la formación indeseada de enona/enal. Las características notables de este método incluyen bajas cargas de catalizador, condiciones de reacción suaves, y sobre todo buena diastereoselectividad.
L. Ye, L. Zhang, Org. Lett., 2009,11, 3646-3649.

Una yodación regio- y estereoselectiva, junto con algunos ejemplos para la bromación, de acrilamidas fácilmente disponibles procede en condiciones suaves a través de un mecanismo de activación/halogenación C-H catalizado por Rh(III). La reacción representa un raro ejemplo de halogenación directa de derivados de ácido acrílico pobres en electrones para acceder a una variedad de derivados de ácido Z-haloacrílico con diferentes sustituciones.
N. Kuhl, N. Schröder, F. Glorius, Org. Lett., 2013,15, 3860-3863.

En una reacción en cascada de adición de aliloxilo-reordenación de Claisen-hidrobromación promovida por NBS, se hicieron reaccionar más de 20 alquilsulfonamidas sustituidas con alcoholes alílicos para generar (2Z)-2,4-dienamidas en buenos rendimientos. Los cálculos teóricos sugieren que un reordenamiento sigmatrópico es el paso que limita la velocidad.
R. Ding, Y. Li, C. Tao, B. Cheng, H. Zhai, Org. Lett., 2015,17, 3994-3997.

Un procedimiento rápido y conveniente de un solo paso permite la conversión de compuestos carbonílicos α,β-insaturados en sus correspondientes bromo-enonas a temperatura ambiente bajo condiciones muy suaves en altos rendimientos utilizando NBS-Et3N – 3 HBr en presencia de carbonato de potasio en diclorometano.
D. Jyothi, S. HariPrasad, Synlett, 2009, 2309-2311.

Se logró una cianoimidación suave, en una sola olla, de aldehídos utilizando cianamida como fuente de nitrógeno y NBS como oxidante en altos rendimientos sin la adición de un catalizador. Posteriormente, los productos de N-cianobenzimidato sustituido también pueden someterse a una reacción de ciclación para dar derivados de 1,2,4-triazol en altos rendimientos.
P. Yin, W.-B. Ma, Y. Chen, W.-C. Huang, Y. Deng, L. He, Org. Lett., 2009,11, 5482-5485.

El Sm(OTf)3 es un catalizador eficaz para una alquilación Friedel-Crafts (F-C) versátil y eficiente promovida por halógenos y altamente regio y estereoselectiva de arenos ricos en electrones con alquenos y compuestos carbonílicos α,β-insaturados en presencia de NBS o I2 como fuentes de halógeno.
S. Haira, B. Maji, S. Bar, Org. Lett., 2007,9, 2783-2786.

Una nueva reacción de difuncionalización altamente regio- y estereoselectiva catalizada por plata de alquinos terminales simples da derivados de acetato de (Z)-β-haloenol en buenos rendimientos. Los productos resultantes son intermedios versátiles en la síntesis orgánica.
Z. Chen, J. Li, H. Jiang, S. Zhu, Y. Li, C. Qi, Org. Lett., 2010,12, 3262-3265.

Un nuevo procedimiento para la aminobromación de olefinas da derivados vicinales de bromoamina en altos rendimientos utilizando catalizadores de Cu, Mn o Vc conp-toluenosulfonamida como fuente de nitrógeno y N-bromosuccinimida(NBS) como fuente de bromo. Se ha demostrado una excelente regioselectividad y estereoselectividad para diferentes sustratos olefínicos, así como para los catalizadores de metales de transición.
V. V. Thakur, S. K. Talluri, A. Sudalai, Org. Lett., 2003,5, 861-864.

Se ha desarrollado una conveniente y eficiente aminobromación de alquenos catalizada por hierro utilizando el barato FeCl2 como catalizador, amidas/sulfonamidas y NBS como fuentes de nitrógeno y bromo, respectivamente, bajo condiciones suaves.
Z. Wang, Y. Zhang, H. Fu, Y. Jiang, Y. Zhao, Synlett, 2008, 2667-2668.

En una bromoamidación eficiente, sin catalizador y sin metales de olefinas no activadas, se utilizaron 4-(trifluorometil)bencenosulfonamida y N-bromosuccinimida como fuentes de nitrógeno y halógeno, respectivamente. La metodología es aplicable tanto a olefinas cíclicas como alifáticas.
W. Z. Yu, F. Chen, Y. A. Cheng, Y.-Y. Yeung, J. Org. Chem., 2015,80, 2815-2821.

Una eficiente reacción de acoplamiento cruzado radical sin catalizador entre aldehídos aromáticos y sulfoximinas tuvo lugar en presencia de N-bromosuccinimida como iniciador radical bajo irradiación de microondas para proporcionar las correspondientes sulfoximinas aciladas en buenos rendimientos.
K. K. Rajbongshi, S. Ambala, T. Govender, H. G. Kruger, P. I. Arvidsson, T. Naicker, Synthesis, 2020, 52, 1279-1286.

Una novedosa reacción electrofílica de una sola vez de una olefina, una ciananina, una amina y N-bromosuccinimida permite la síntesis de varios derivados de guanidina con muy buenos rendimientos – incluyendo un precursor de rTRTVI.
L. Zhou, J. Chen, J. Zhou, Y.-Y. Yeung, Org. Lett., 2011,13, 5804-5807.

Una arilación y vinilación estereoselectiva de alquenos sin catalizadores de metales de transición tiene lugar a través de un interesante reordenamiento de semipinacol promovido por NBS en condiciones suaves y una posterior fragmentación inusual de Grob mediada por NaOH.
D.-Y. Yuan, Y.-Q. Tu, C.-A. Fan, J. Org. Chem., 2008,73, 7797-7799.

Una novedosa síntesis iniciada por Br catiónico en un solo paso utilizando olefina, nitrilo, amina y N-bromosuccinimida da imidazolinas en buenos rendimientos. Los sustratos olefínicos y los socios nitrilos pueden variarse de forma flexible para conseguir una gama de derivados de imidazolina.
L. Zhou, J. Zhou, C. K. Tan, J. Chen, Y.-Y. Yeung, Org. Lett., 2011,13, 2448-2451.

Una síntesis directa mediada por N-bromosuccinimida de 2,5-diariloxazoles a partir de N-H cetoaziridinas procede a través de la formación in situ de N-bromoketoaziridinas seguida de la generación de ylides de azometa.
H. S. Samimi, F. Dadvar, Synthesis, 2015, 47, 1899-1904.

Los 3-oxazolina-4-carboxilatos como intermedios sintéticos fácilmente disponibles pueden ser oxidados para producir oxazol-4-carboxilatos. Además, la derivatización de 3-oxazolina-4-carboxilatos con reactivos de Grignard permite una preparación fácil de derivados de 4-keto-oxazol.
K. Murai, Y. Takahara, T. Matsushita, H. Komatsu, H. Fujioka, Org. Lett., 2010,12, 3456-3459.

Los 2-amino-4-alquil- y 2-amino-4-ariltiazol-5-carboxilatos y sus análogos de selenazol se sintetizaron por α-halogenación de β-cetoesteres con N-bromosuccinimida, seguida de ciclación con tiourea o selenourea, respectivamente, en presencia de β-ciclodextrina en agua a 50°C.
M. Narender, M. S. Reddy, V. P. Kumar, B. Srinivas, R. Sridhar, Y. V. D. Nageswar, K. R. Rao, Synthesis, 2007, 3469-3472.
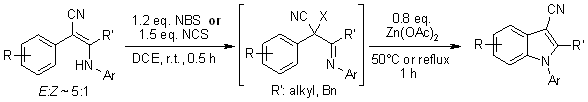
Varios 2-aril-3-arilamino-2-alquenitrilos dan N-arilindol-3-carbonitrilos de una sola vez a través de la halogenación mediada por NBS o NCS seguida de la ciclización intramolecular catalizada por Zn(OAc)2. El proceso implica la formación de intermedios de iones de arilnitrio, que se someten a una sustitución aromática electrofílica para dar los N-arilindoles ciclizados.
Q. Yan, J. Luo, D. Zhang-Negrerie, H. Li, X. Qi, K. Zhao, J. Org. Chem., 2011,76, 8690-8697.

Los sulfoxidos de terceto pueden utilizarse como fuentes de sulfinilo en una sulfinilación intramolecular de sulfonamidas seguida de un proceso equivalente a Wittig de todos los heteroátomos para obtener arilisotiazoles en altos rendimientos.
F. Xu, Y. Chen, E. Fan, Z. Sun, Org. Lett., 2016, 18, 2777-2779.

Una ciclización halogenativa sin catalizador de diazoamidas de N-arilo con N-halosuccinimidas (NXS) proporciona 3-halooxindoles en buenos rendimientos a través de un mecanismo sin carbenos en condiciones suaves y sin catalizador. Se propone que esta transformación procede a través de la formación de iones de diazonio seguida de una alquilación intramolecular de Friedel-Crafts.
C. Ma, D. Xing, W. Hu, Org. Lett., 2016, 18, 3134-3137.

Se describe una nueva metodología para la síntesis de 2-oxazolinas diversamente sustituidas y una dihidrooxazina utilizando aldehídos, amino alcoholes y N-bromosuccinimida como agente oxidante. Esta síntesis de una sola olla se caracteriza por sus condiciones de reacción suaves, su amplio alcance, sus altos rendimientos y su simplicidad preparativa.
K. Schwekendiek, F. Glorius, Synthesis, 2006, 2996-3002.

Una ciclización catalizada por oro de intermedios de β-amino-ynona y un proceso de halodeuración permite una síntesis de halopiridona de un paso rápida y eficiente.
K. H. Nguyen, S. Tomasi, M. Le Roch, L. Toupet, J. Renault, P. Uriac, N. Gouault, J. Org. Chem., 2013,78, 7809-7815.

Una reacción versátil y altamente eficiente de alquenos, NBS, nitrilos y TMSN3 catalizada por Zn(OTf)2 en un solo paso da lugar a varios tetrazoles 1,5-disustituidos que contienen una funcionalidad α-bromo adicional del sustituyente N1-alquilo.
S. Hajra, D. Sinha, M. Bhowmick, J. Org. Chem., 2007,72, 1852-1855.

Se describe una síntesis en una sola olla de aril sulfonas a partir de alcoholes primarios. Los alcoholes se trataron con N-bromosuccinimida y trifenilfosfina, seguido de la adición de arenesulfinato de sodio con una cantidad catalítica de yoduro de tetrabutilamonio para obtener las aril sulfonas en rendimientos buenos a altos.
T. Murakami, K. Furusawa, Synthesis,2002, 479-482.

Los sulfóxidos que llevan un grupo tert-butil pueden activarse utilizando N-bromosuccinimida (NBS) en condiciones ácidas. El tratamiento posterior con varios nucleófilos de nitrógeno, carbono u oxígeno proporciona una amplia gama de amidas de ácido sulfínico, nuevos sulfóxidos y ésteres de ácido sulfínico.
J. Wei, Z. Sun, Org. Lett., 2015,17, 5396-5399.

El cianuro media una generación in situ de un ion sulfato nucleófilo a partir de sulfonas de vinilo. La posterior S-alquilación in situ proporciona sulfonas en altos rendimientos. En presencia de N-bromosuccinimida, las aminas primarias y secundarias sufrieron la formación de sulfonamidas.
T. Roy, J.-W. Lee, Synlett, 2020, 31, 455-458.

Los tiosulfonatos sintetizados por dimerización aeróbica catalizada por cobre sirven como sustrato para estrategias simples y de alto rendimiento para la producción de una variedad de sulfonas y sulfonamidas. Los tiosulfinatos son alternativas estables y no tóxicas a las sales metálicas de sulfato derivadas del tóxico SO2.
P. K. Shyam, H.-Y. Jang, J. Org. Chem., 2017, 82, 1761-1767.

La síntesis de N-cianosulfiliminas puede lograrse fácilmente mediante la reacción de los sulfuros correspondientes con amina cianógena en presencia de una base y NBS o I2 como agentes halogenantes. La oxidación seguida de la descianización proporciona sulfoximinas sintéticamente útiles.
O. García Mancheño, O. Bistri, C. Bolm, Org. Lett., 2007,9, 3809-3811.

En una transformación en cascada de una sola vez de cetonas en α-imidoketonas, la N-bromosuccinimida (NBS) proporciona tanto bromo electrofílico como fuentes de nitrógeno nucleofílico, y el diazabicicloundec-7-eno (DBU) funciona como base y promotor nucleofílico para la activación de la NBS. Se supone que la α-bromación es el paso clave del proceso.
Y. Wei, S. Lin, F. Liang, Org. Lett., 2012,14, 4202-4205.