By Drew Jones MD, Laleh Gharahbaghian MD & Viveta Lobo MD
Fino a poco tempo fa, la funzione del cuore destro e il suo ruolo in molti processi patologici era sottovalutata. Anche ora, quando riconosciamo l’importanza dell’aumento del postcarico del ventricolo destro (RV) nell’embolia polmonare e nell’ipertensione polmonare cronica, la diminuzione del precarico del RV nel tamponamento e negli stati di shock, e/o la diminuzione della contrattilità nell’infarto del RV, la valutazione rapida del cuore destro al letto del paziente rimane sfuggente. La risonanza magnetica cardiaca è diventata il gold standard della cardiologia nella valutazione della funzione del cuore destro, ma è impraticabile nel paziente instabile comunemente visto nel dipartimento di emergenza. I marcatori surrogati della funzione della RV come l’escursione sistolica del piano anulare della tricuspide (TAPSE) e la velocità di escursione sistolica (S’) sono promettenti come un aumento rapido e facilmente eseguibile dell’ecocardiogramma al letto del paziente. Entrambi hanno dei limiti, vale a dire, entrambi valutano la funzione della RV in un singolo piano e sono quindi specifici ma non sensibili per la disfunzione della RV. Quando vengono utilizzati con i marcatori della dilatazione del cuore destro, dell’aumento della pressione e dell’ipertrofia della RV, i marcatori surrogati della funzione della RV aiutano nella diagnosi, nella stratificazione del rischio e nella gestione del paziente acutamente dispneico.1-3
Una delle minacce immediate per la vita che il medico di emergenza deve considerare nel paziente acutamente dispneico è l’embolia polmonare (PE). L’EP rimane una delle eziologie più comuni di disfunzione cardiopolmonare e di morte con un’incidenza annuale di circa 1:1000 e una mortalità che si avvicina al 15% nella popolazione statunitense.4-5 Inoltre, rimane una diagnosi elusiva con un numero significativo di emboli polmonari clinicamente rilevanti ma insospettabili trovati sull’autopsia post-mortem.6 Il grado di compromissione emodinamica sistemica è correlato a una maggiore morbilità e mortalità nei pazienti con embolia polmonare acuta. Questo vale anche per i pazienti normotesi, con una disfunzione cardiaca destra acuta che conferisce un aumento di due-dieci volte della mortalità a breve termine.7 L’ecocardiogramma eseguito dal medico d’urgenza può aumentare l’esame fisico, l’ECG e i biomarcatori per identificare rapidamente questi pazienti, guidare le decisioni di gestione e la disposizione finale.
Consigli per la valutazione del cuore destro:
1. Sonda: phased array
2. Utilizzare le tradizionali 4 viste ecocardiografiche limitate: asse lungo parasternale (PSLA), asse corto parasternale (PSSA), 4 camere apicali (A4C), sub-xifoide
3. Asse corto parasternale:
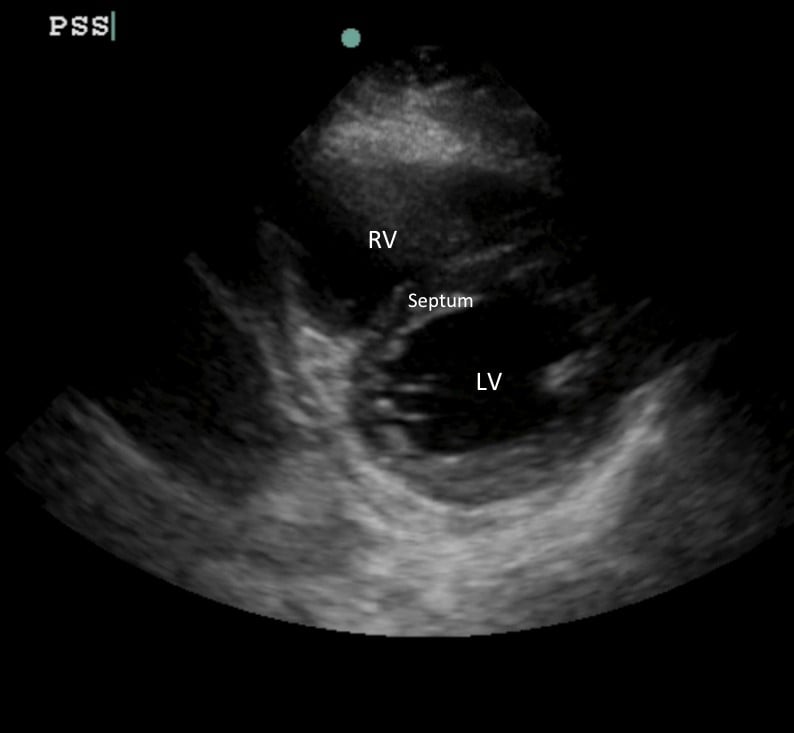
Immagine 1: RV normale a mezzaluna e LV concentrico
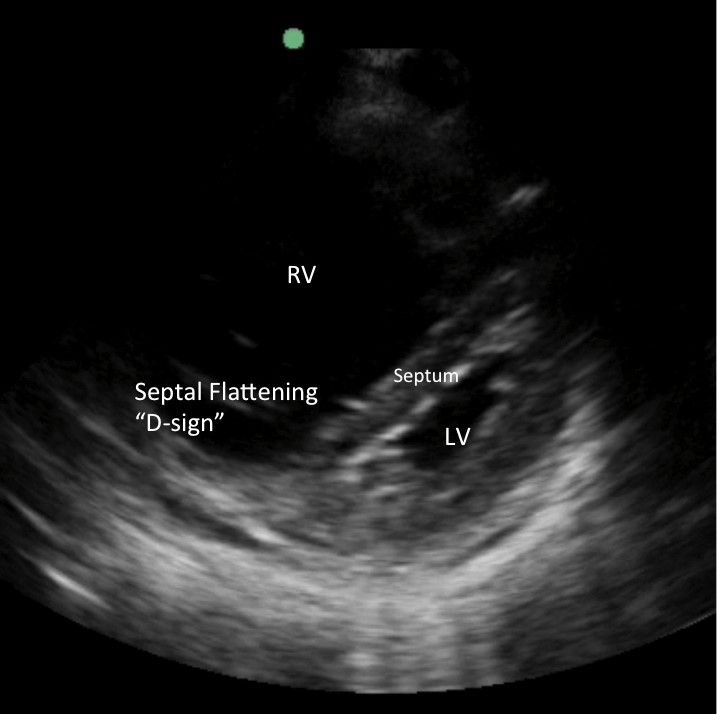
Immagine 2: RHS che mostra RV arrotondato e dilatato e appiattimento del setto interventricolare durante la diastole (“D-sign” causato dall’aumento della pressione RV)
4. Apicale 4 camere:
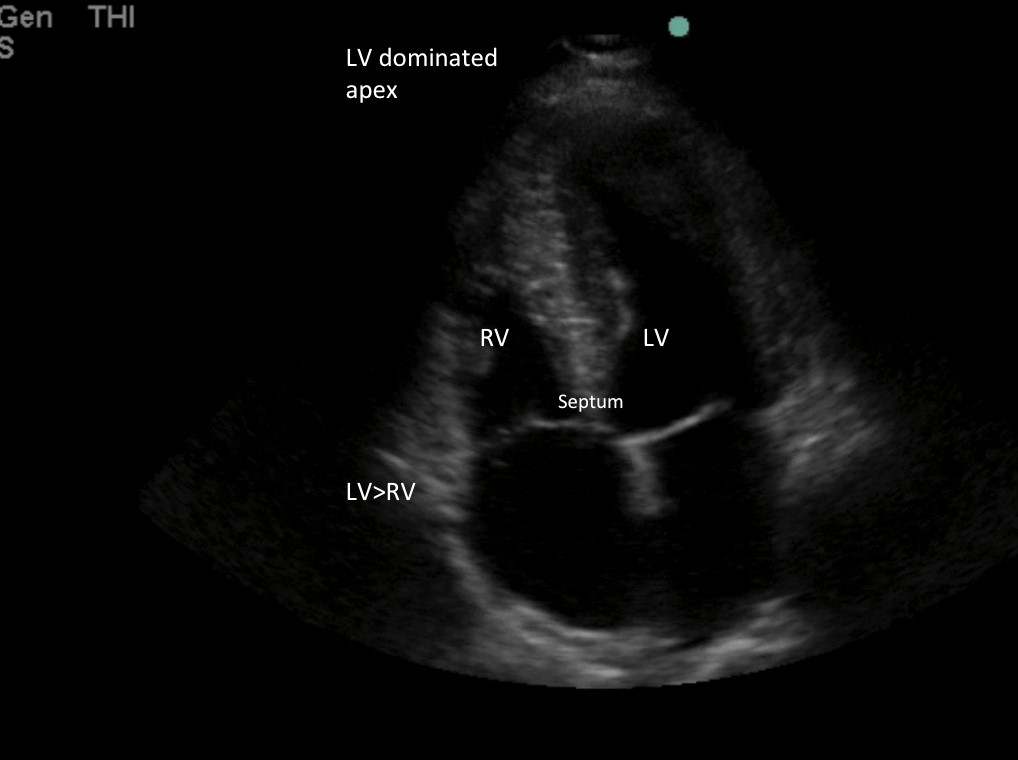
Immagine 3: Dimensione normale della RV inferiore a ⅔ della dimensione del LV e apice dominato dal LV
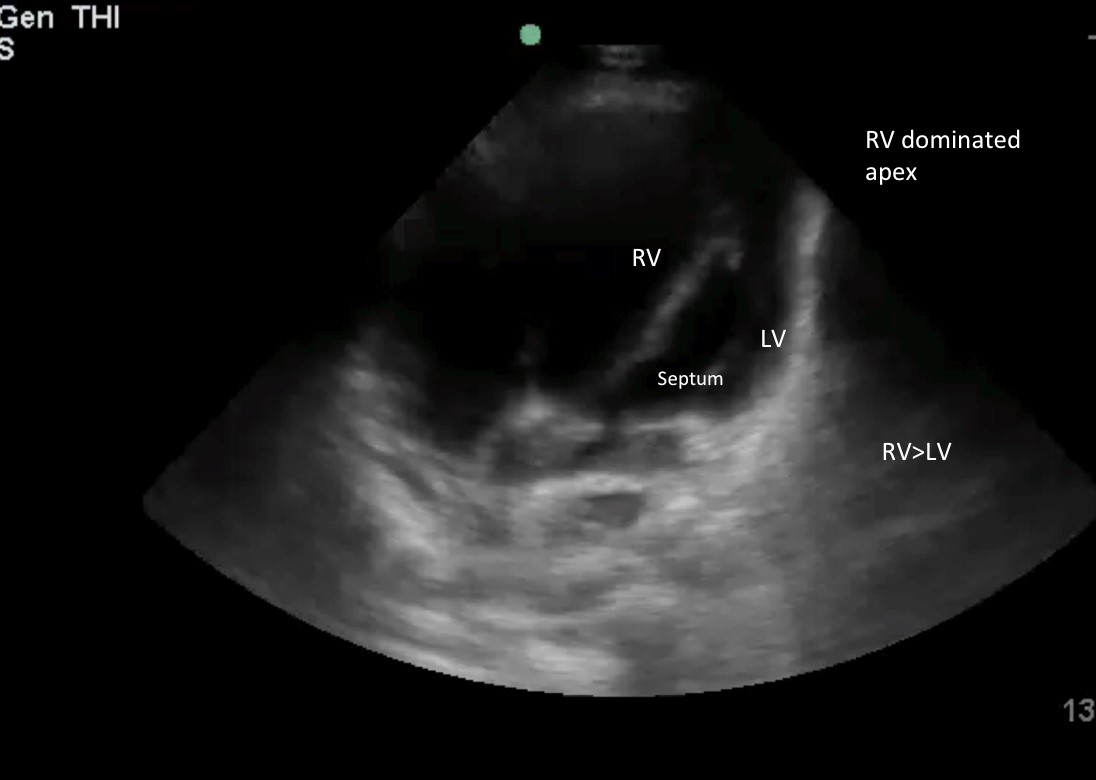
Immagine 4: Dimensione RV > ⅔ della dimensione del LV e apice dominato dal RV
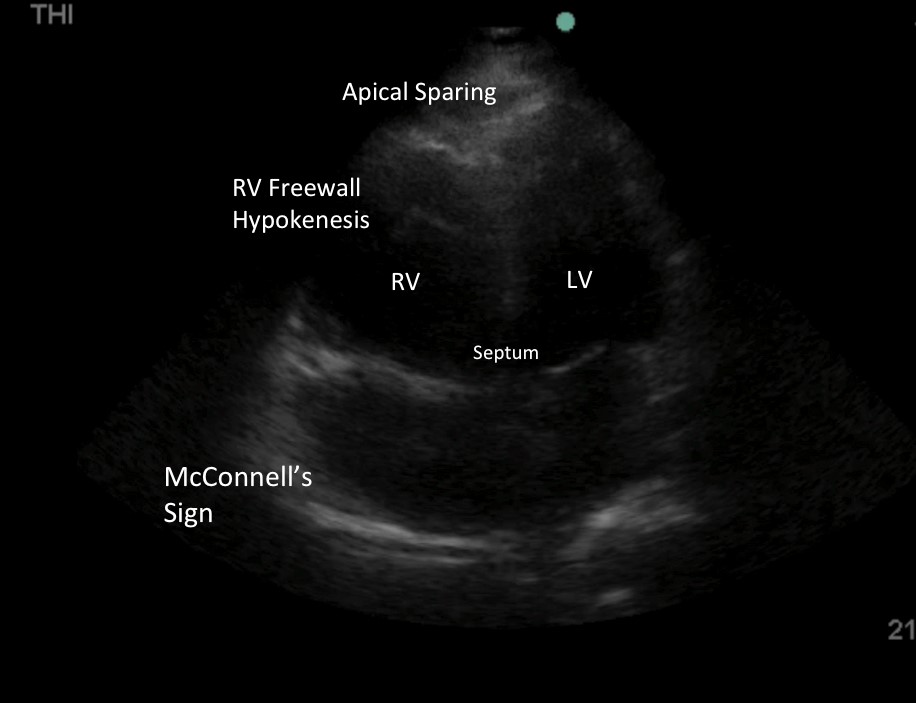
Immagine 5: Segno di McConnell: Ipocinesi della parete libera di RV con compressione apicale conservata. I dati originali hanno suggerito che il segno di McConnell era un indicatore specifico di PE acuta in contrasto con l’ipo-cinesia più uniforme previsto in ipertensione polmonare cronica primaria o secondaria (PHTN). Dati recenti confutano questa conclusione in quanto il segno di McConnell si osserva nella PHTN.8-9
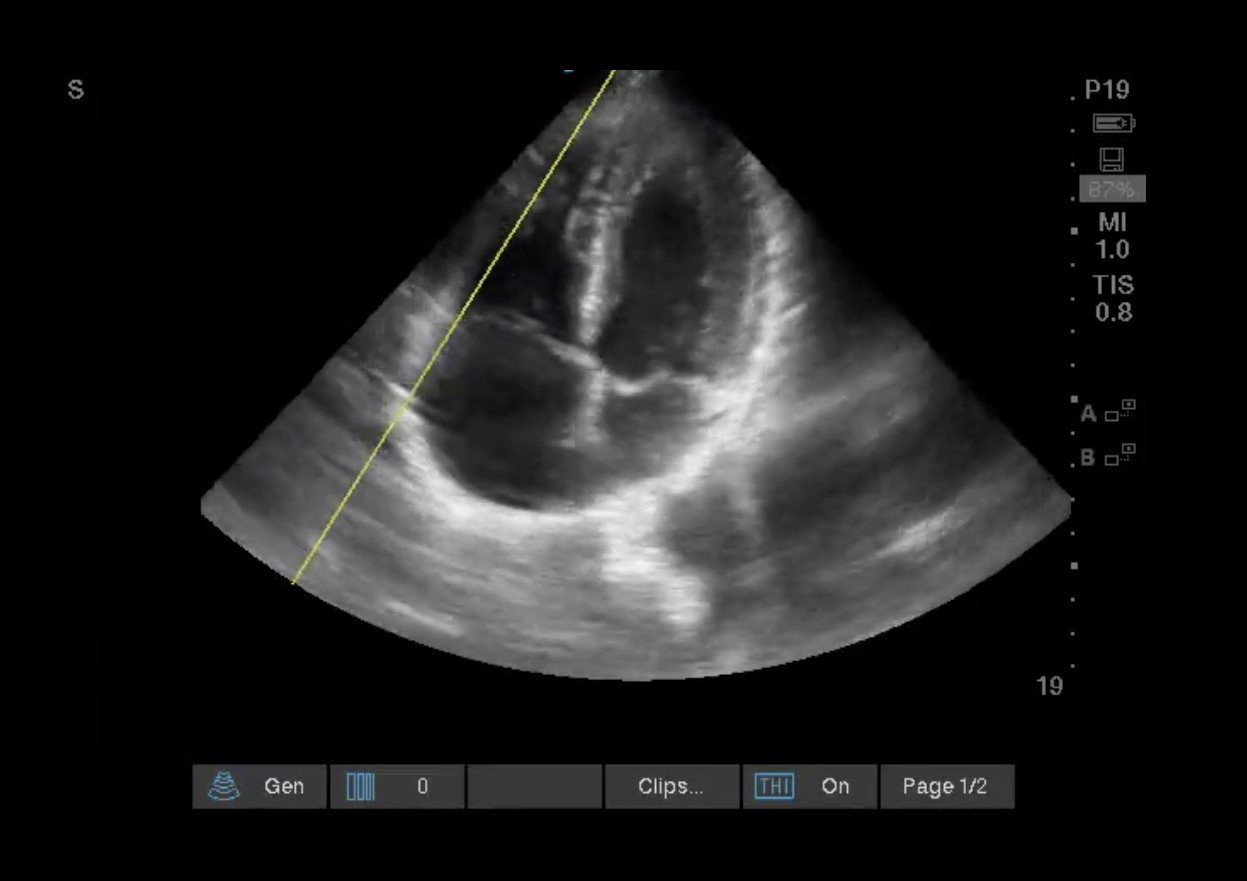
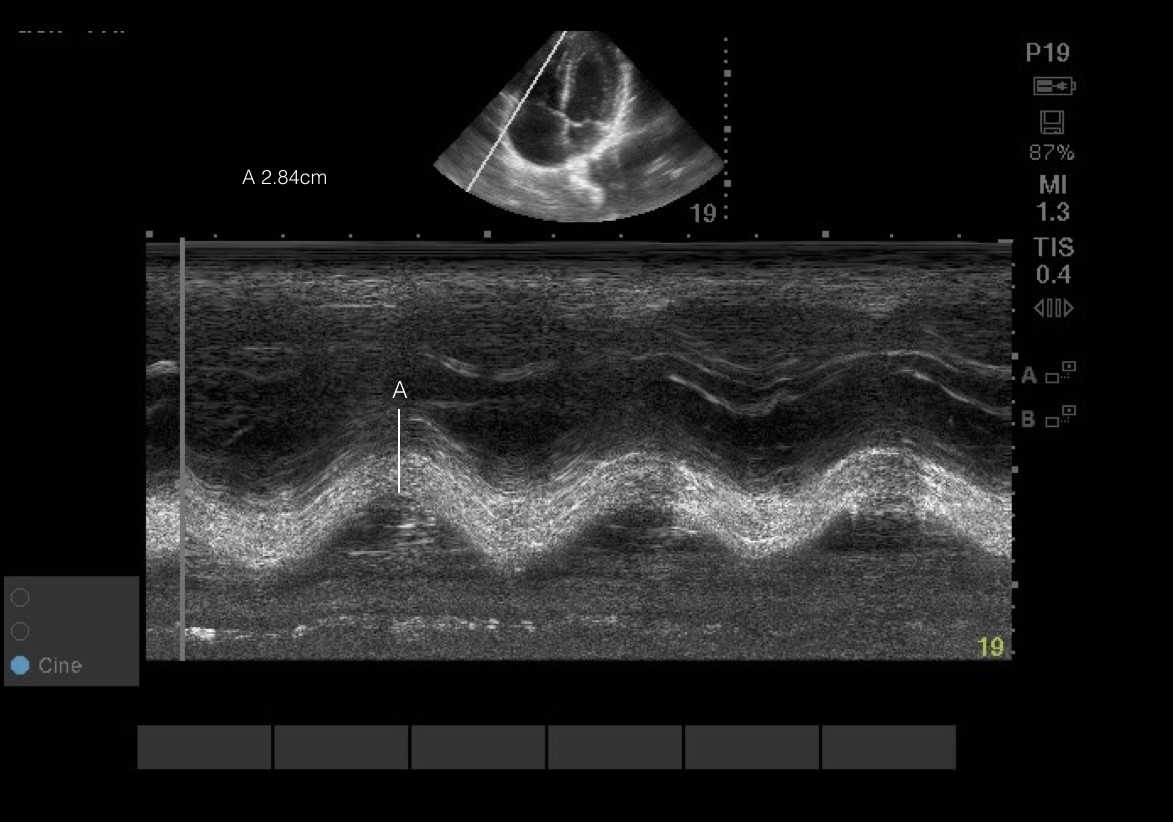
Immagini 6, 7 & Video 1 TAPSE: Il RV si contrae principalmente sul piano longitudinale dall’apice alla base. Pertanto, la valutazione del movimento libero laterale verso e lontano dalla sonda (TAPSE) e la forza di questa contrazione (S’) permette loro di agire come marcatori surrogati della funzione sistolica RV. Per eseguire, posizionare il cursore M-mode attraverso la parete libera laterale a livello dell’anulus tricuspide per ottenere un’onda sin. Misurare da picco a valle o massima escursione sistolica e diastolica. TAPSE anomalo<16mm. Per S’: posizionare il doppler a onde di polso sulla parete libera laterale appena distale all’anulus laterale. Misurare la velocità massima sopra la linea di base. S’ anormale < 9.5cm/s
Pitfalls: TAPSE e S’ sono dipendenti dall’angolo. Pertanto, la loro capacità di valutare la funzione RV si degrada significativamente sulle viste A4C di scarsa qualità. Inoltre, questi marcatori surrogati valutano solo la RV in un piano; i pazienti possono avere disfunzioni significative della RV con TAPSE/S’ normali. Nonostante queste limitazioni, TAPSE/S’ correlano con la morbilità nell’insufficienza della RV dei pazienti con HTN polmonare.
5. Sub-xifoide (nessuna immagine)
La misurazione della parete libera laterale in primo piano può dare un senso di cronicità della malattia. Normale <5mm, maggiore di 5mm indicativo di RHS cronica.
Pitfall: i pazienti con insufficienza cardiaca cronica possono scompensare acutamente. Pertanto, la misura della parete libera è meglio usata come “escludere la RHS cronica” se <5mm rispetto allo strumento “rule in”.
Conclusione
Preso nella sua totalità: la valutazione della dilatazione ventricolare destra, il movimento anomalo del setto, l’ipocinesi della parete libera del ventricolo destro e i marcatori surrogati della funzione sistolica del RV permettono al medico di emergenza di valutare rapidamente la funzione del cuore destro e di iniziare la terapia salvavita.
1. Ryan JJ, Tedford RJ. Diagnosi e trattamento del cuore destro in crisi. Curr Opin Cardiol. 2015;30(3):292-300.
2. Soni NJ, Arntfield R, Kory P. Point of Care Ultrasound E-book. Elsevier Health Sciences, 2014, 110-118.
3. Kossaify A. Valutazione ecocardiografica del ventricolo destro, dall’approccio convenzionale allo speckle tracking e all’imaging tridimensionale, e approfondimenti sul “Right Way” per esplorare la camera dimenticata. Clin Med Insights Cardiol. 2015;9:65-75.
4. Silverstein MD, Heit JA, Mohr DN, et al. Trends in the incidence of deep vein thrombosis and pulmonary embolism: a 25-year population-based study. Arch Intern Med. 1998; 158: 585-93.
5. Horlander KT, Mannino DM, Leeper KV. Mortalità per embolia polmonare negli Stati Uniti, 1979-1998. Un’analisi utilizzando i dati di mortalità per cause multiple. Arch Intern Med. 2003;163(14):1711-1717. doi:10.1001/archinte.163.14.1711
6. Stein PD, Henry JW. Prevalenza di embolia polmonare acuta tra i pazienti di un ospedale generale all’autopsia. Chest. 1995; 108: 978-81.
7. Matthews JC, McLaughlin V. Insufficienza ventricolare destra acuta nell’impostazione di embolia polmonare acuta o ipertensione polmonare cronica: Una revisione dettagliata della fisiopatologia, diagnosi e gestione. Curr Cardiol Reviews. 2008, 4, 49-59.
8. Mediratta A, Addetia K, Medvedofsky D, et al. diagnosi ecocardiografica di embolia polmonare acuta in pazienti con segno di McConnell. Ecocardiografia. 2016;33(5):696-702. doi:10.1111/echo.13142.
9. Walsh BM, Moore CL. Il segno di McConnell non è specifico per l’embolia polmonare: Case report e revisione della letteratura. J Emerg Med. 2015;49(3):301-304.
10. Daley J, Grotberg J, Pare J, et al. Medico di emergenza eseguito tricuspide escursione sistolica piano anulare nella valutazione di sospetta embolia polmonare. Am J Emerg Med. 2017;35:106-111.
Ritorna alla newsletter