Por Drew Jones MD, Laleh Gharahbaghian MD & Viveta Lobo MD
Hasta hace poco, la función del corazón derecho y su papel en muchos procesos patológicos estaba infravalorada. Incluso ahora, cuando reconocemos la importancia del aumento de la poscarga del ventrículo derecho (VD) en la embolia pulmonar y la hipertensión pulmonar crónica, la disminución de la precarga del VD en el taponamiento y los estados de shock, y/o la disminución de la contractilidad en el infarto del VD, la evaluación rápida del corazón derecho a pie de cama sigue siendo difícil. La resonancia magnética cardíaca se ha convertido en el estándar de oro de la cardiología para evaluar la función del corazón derecho, pero no es práctica en el paciente inestable que se ve habitualmente en el servicio de urgencias. Los marcadores sustitutivos de la función del VD, como la excursión sistólica del plano anular tricuspídeo (TAPSE) y la velocidad de excursión sistólica (S’), resultan prometedores como complemento rápido y sencillo del ecocardiograma de cabecera. Ambos tienen limitaciones, a saber, ambos evalúan la función del VD en un solo plano y, por lo tanto, son específicos pero no sensibles para la disfunción del VD. Cuando se utilizan con marcadores de dilatación del corazón derecho, aumento de la presión e hipertrofia del VD, los marcadores sustitutos de la función del VD ayudan al diagnóstico, la estratificación del riesgo y el tratamiento del paciente con disnea aguda.1-3
Una de las amenazas vitales inmediatas que el médico de urgencias debe tener en cuenta en el paciente con disnea aguda es la embolia pulmonar (EP). La embolia pulmonar sigue siendo una de las etiologías más comunes de la disfunción cardiopulmonar y de la muerte, con una incidencia anual de aproximadamente 1:1000 y una mortalidad que se aproxima al 15% en la población de EE.UU., respectivamente.4-5 Además, sigue siendo un diagnóstico elusivo con un número significativo de embolias pulmonares clínicamente relevantes pero insospechadas encontradas en la autopsia post-mortem.6 El grado de compromiso hemodinámico sistémico se correlaciona con un aumento de la morbilidad y la mortalidad en pacientes con embolia pulmonar aguda. Esto también es cierto en los pacientes normotensos, ya que la disfunción aguda del corazón derecho multiplica por dos la mortalidad a corto plazo.7 El ecocardiograma de cabecera realizado por los médicos de urgencias puede aumentar la exploración física, el electrocardiograma y los biomarcadores para identificar rápidamente a estos pacientes, guiar las decisiones de tratamiento y la disposición final.
Consejos para la evaluación del corazón derecho:
1. Sonda: phased array
2. Utilizar las tradicionales 4 vistas limitadas del ecocardiograma: eje largo paraesternal (ALP), eje corto paraesternal (EPA), apical de 4 cámaras (A4C), subxifoidea
3. Eje corto paraesternal:
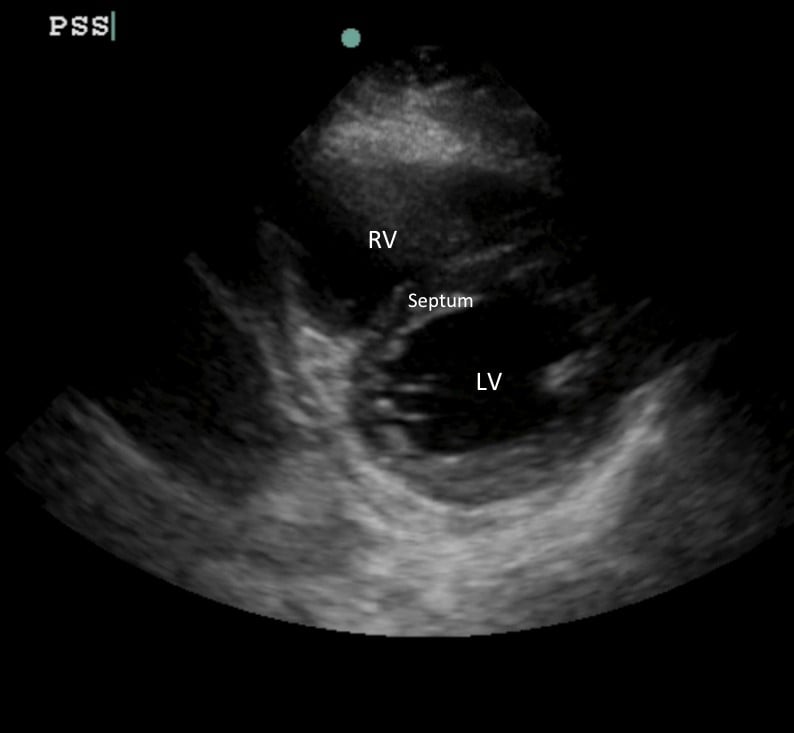
Imagen 1: VD normal en forma de media luna y VI concéntrico
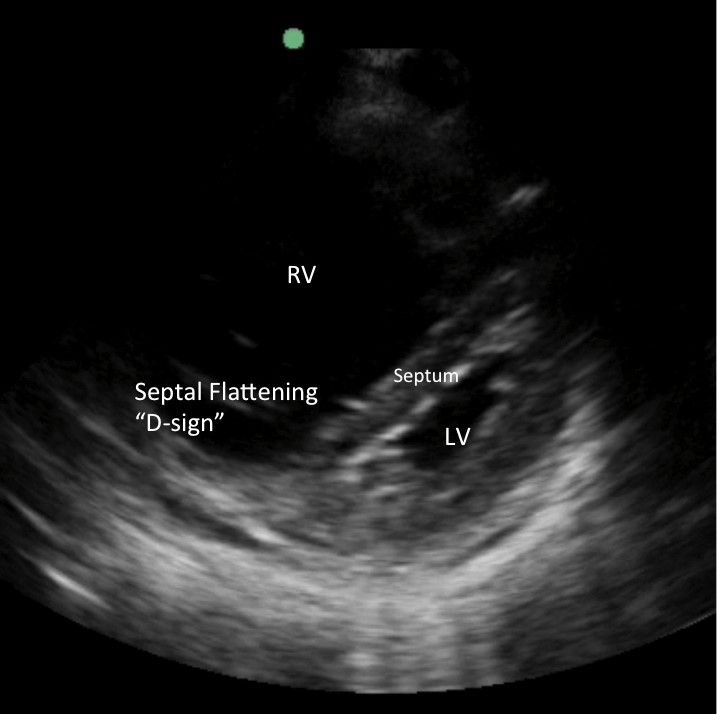
Imagen 2: RHS que muestra un VD redondeado y dilatado y un aplanamiento del tabique interventricular durante la diástole («signo D» causado por el aumento de la presión del VD)
4. Cámara 4 apical:
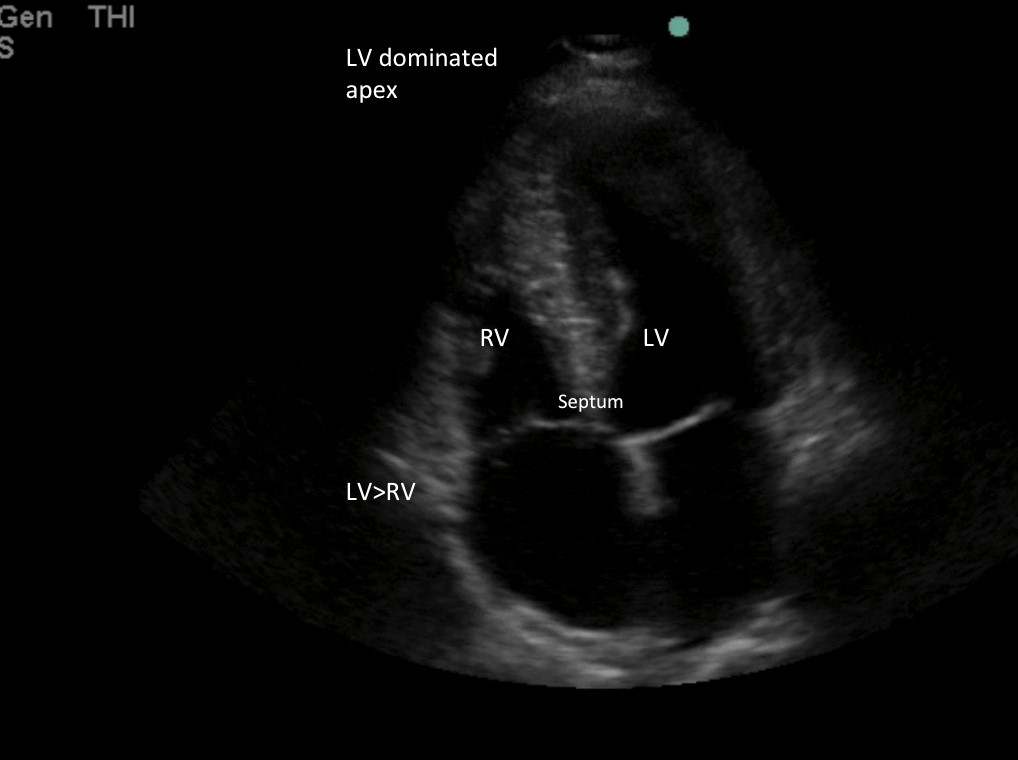
Imagen 3: Tamaño normal del VD inferior a ⅔ del tamaño del VI y ápice dominado por el VI
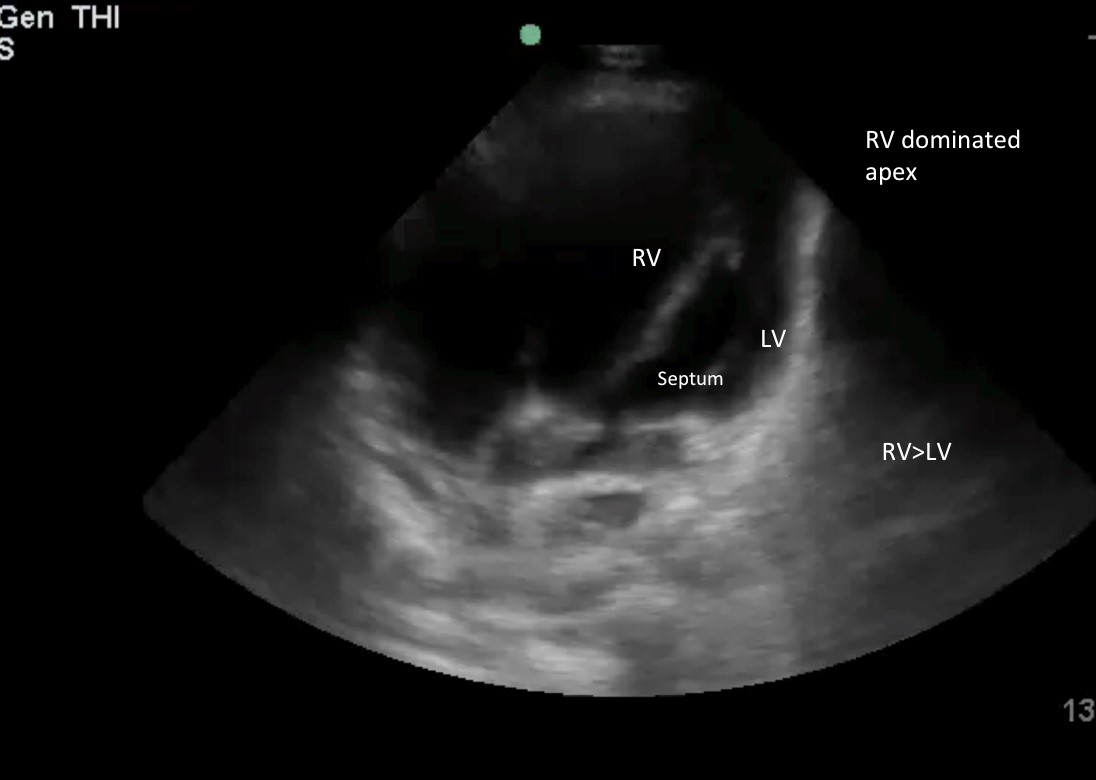
Imagen 4: Tamaño del VD > ⅔ del tamaño del VI y vértice dominado por el VD
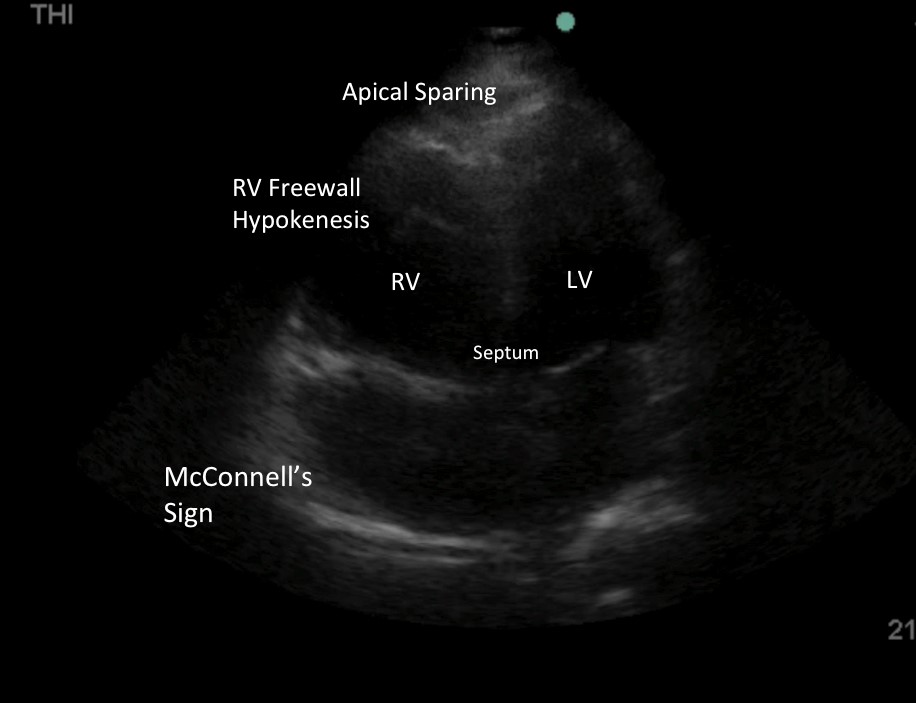
Imagen 5: Signo de McConnell: Hipocinesia de la pared libre del VD con compresión apical conservada. Los datos originales sugerían que el signo de McConnell era un indicador específico de la EP aguda en contraposición a la hipoquinesis más uniforme que se espera en la hipertensión pulmonar crónica primaria o secundaria (HPTN). Datos recientes refutan esta conclusión, ya que el signo de McConnell se observa en la HTP.8-9
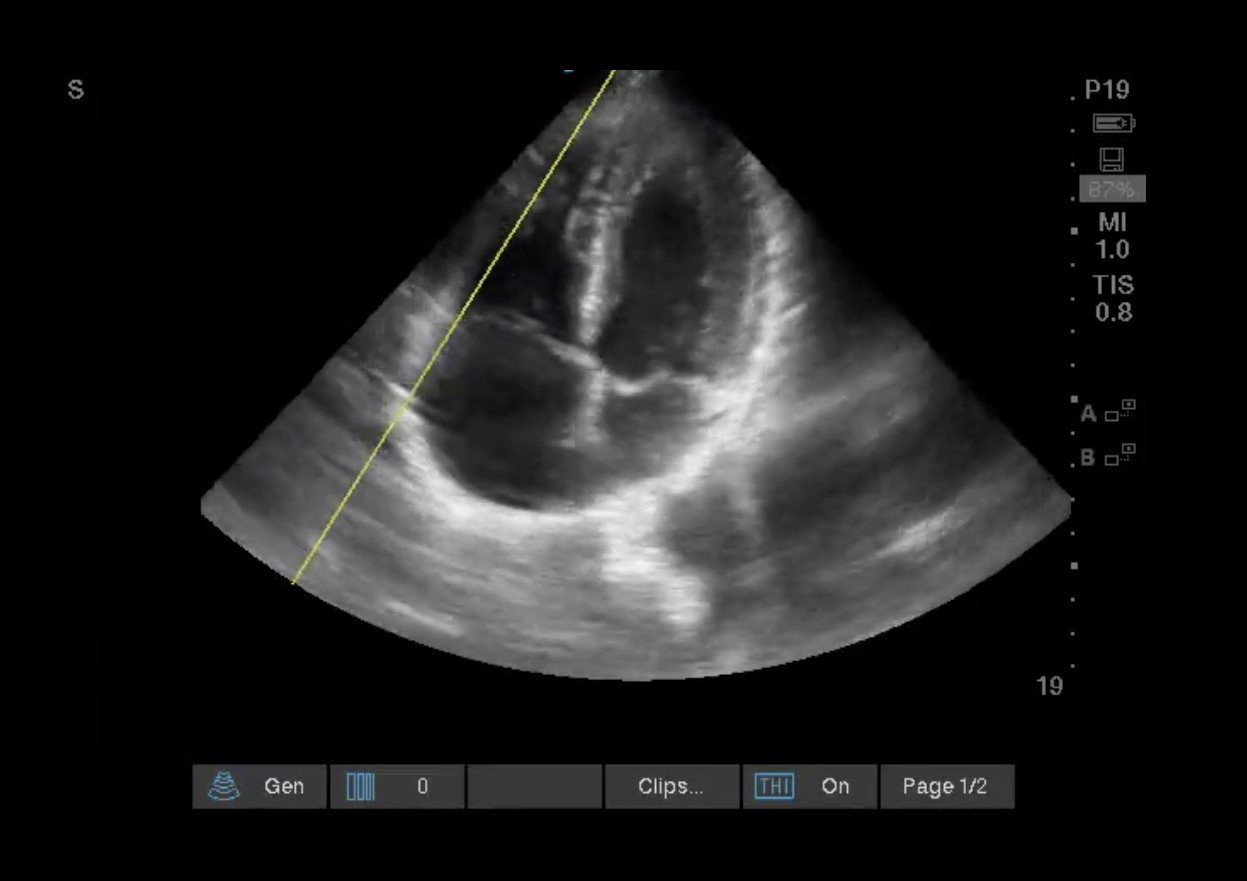
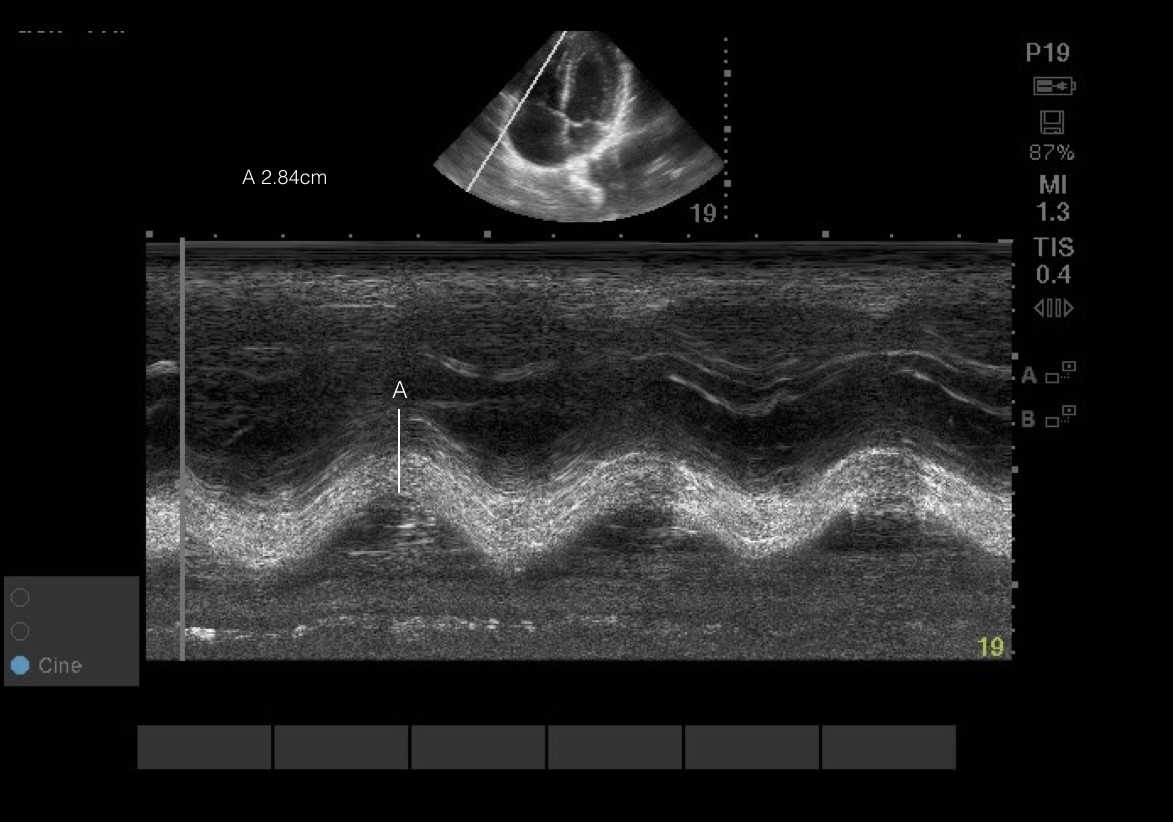
Imágenes 6, 7 & Vídeo 1 TAPSE: El VD se contrae principalmente en el plano longitudinal desde el ápice hasta la base. Por lo tanto, la evaluación del movimiento libre lateral hacia y desde la sonda (TAPSE) y la fuerza de esta contracción (S’) permiten actuar como marcadores sustitutos de la función sistólica del VD. Para ello, coloque el cursor en modo M a través de la pared libre lateral a nivel del anillo tricúspide para obtener una onda sin. Medir desde el pico hasta el valle o la máxima excursión sistólica y diastólica. TAPSE anormal<16mm. Para S’: colocar el doppler de onda de pulso sobre la pared libre lateral justo distal al anillo lateral. Medir la velocidad máxima por encima de la línea de base. S’ anormal < 9,5cm/s
Peligros: El TAPSE y el S’ son dependientes del ángulo. Por lo tanto, su capacidad para evaluar la función del VD se degrada significativamente en vistas A4C de mala calidad. Además, estos marcadores sustitutivos sólo evalúan el VD en un plano; los pacientes pueden tener una disfunción significativa del VD con TAPSE/S’ normales. A pesar de estas limitaciones, los TAPSE/S’ se correlacionan con la morbilidad en la insuficiencia del VD de los pacientes con HTA pulmonar.
5. Sub-xifoidea (sin imágenes)
La medición de la pared libre lateral en primer plano puede dar alguna idea de la cronicidad de la enfermedad. Normal <5mm, Mayor de 5mm indica RHS crónico.
Peligro: los pacientes con insuficiencia cardiaca crónica pueden descompensarse de forma aguda. Por lo tanto, la medición de la pared libre se utiliza mejor como herramienta para «descartar el RHS crónico» si <5mm que para «descartar».
Conclusión
Tomado en su totalidad: la evaluación de la dilatación del ventrículo derecho, el movimiento septal anormal, la hipocinesia de la pared libre del ventrículo derecho y los marcadores sustitutos de la función sistólica del VD permiten al médico de urgencias evaluar rápidamente la función del corazón derecho e iniciar una terapia que salve la vida.
1. Ryan JJ, Tedford RJ. Diagnóstico y tratamiento del corazón derecho insuficiente. Curr Opin Cardiol. 2015;30(3):292-300.
2. Soni NJ, Arntfield R, Kory P. Point of Care Ultrasound E-book. Elsevier Health Sciences, 2014, 110-118.
3. Kossaify A. Echocardiographic assessment of the right ventricle, from the conventional approach to speckle tracking and three-dimensional imaging, and insights into the «Right Way» to explore the forgotten chamber. Clin Med Insights Cardiol. 2015;9:65-75.
4. Silverstein MD, Heit JA, Mohr DN, et al. Trends in the incidence of deep vein thrombosis and pulmonary embolism: a 25-year population-based study. Arch Intern Med. 1998; 158: 585-93.
5. Horlander KT, Mannino DM, Leeper KV. Mortalidad por embolia pulmonar en los Estados Unidos, 1979-1998. Un análisis utilizando datos de mortalidad por causas múltiples. Arch Intern Med. 2003;163(14):1711-1717. doi:10.1001/archinte.163.14.1711
6. Stein PD, Henry JW. Prevalencia de la embolia pulmonar aguda entre los pacientes de un hospital general en la autopsia. Chest. 1995; 108: 978-81.
7. Matthews JC, McLaughlin V. Acute right ventricular failure in the setting of acute pulmonary embolism or chronic pulmonary hypertension: Una revisión detallada de la fisiopatología, el diagnóstico y el manejo. Curr Cardiol Reviews. 2008, 4, 49-59.
8. Mediratta A, Addetia K, Medvedofsky D, et al. Echocardiographic diagnosis of acute pulmonary embolism in patients with McConnell’s Sign. Echocardiography. 2016;33(5):696-702. doi:10.1111/echo.13142.
9. Walsh BM, Moore CL. El signo de McConnell no es específico de embolia pulmonar: Informe de un caso y revisión de la literatura. J Emerg Med. 2015;49(3):301-304.
10. Daley J, Grotberg J, Pare J, et al. Excursión sistólica del plano anular tricuspídeo realizada por el médico de emergencias en la evaluación de la sospecha de embolia pulmonar. Am J Emerg Med. 2017;35:106-111.
Volver al boletín