Von Dr. Drew Jones, Dr. Laleh Gharahbaghian & Dr. Viveta Lobo
Bis vor kurzem wurde die Rechtsherzfunktion und ihre Rolle bei vielen Krankheitsprozessen unterschätzt. Selbst jetzt, da wir die Bedeutung einer erhöhten rechtsventrikulären Nachlast bei Lungenembolie und chronischer pulmonaler Hypertonie, einer verminderten RV-Vorlast bei Tamponade und Schockzuständen und/oder einer verminderten Kontraktilität bei RV-Infarkt erkennen, bleibt eine schnelle Bewertung des rechten Herzens am Krankenbett schwer zu erreichen. Die kardiale MRT hat sich zum Goldstandard der Kardiologie bei der Beurteilung der Rechtsherzfunktion entwickelt, ist aber bei instabilen Patienten, die häufig in der Notaufnahme behandelt werden, nicht praktikabel. Surrogatmarker der RV-Funktion wie die Tricuspid Annular Plane Systolic Excursion (TAPSE) und die Systolic Excursion Velocity (S‘) sind vielversprechend als schnelle und einfach durchzuführende Ergänzung des bettseitigen Echokardiogramms. Beide haben jedoch Einschränkungen, nämlich die, dass sie die RV-Funktion in einer einzigen Ebene bewerten und daher zwar spezifisch, aber nicht sensitiv für eine RV-Dysfunktion sind. In Verbindung mit Markern für Rechtsherzdilatation, erhöhten Druck und RV-Hypertrophie helfen Surrogatmarker für die RV-Funktion bei der Diagnose, Risikostratifizierung und Behandlung des akut dyspnoischen Patienten.1-3
Eine der unmittelbaren Lebensbedrohungen, die der Notarzt bei einem akut dyspnoischen Patienten in Betracht ziehen muss, ist die Lungenembolie (PE). Die Lungenembolie ist nach wie vor eine der häufigsten Ursachen für kardiopulmonale Funktionsstörungen und Todesfälle mit einer jährlichen Inzidenz von ca. 1:1000 und einer Mortalität von ca. 15 % in der US-Bevölkerung.4-5 Darüber hinaus bleibt die Diagnose schwer zu fassen, da eine beträchtliche Anzahl klinisch relevanter, aber unverdächtiger Lungenembolien bei der postmortalen Autopsie gefunden wird.6 Der Grad der systemischen hämodynamischen Beeinträchtigung korreliert mit einer erhöhten Morbidität und Mortalität bei Patienten mit akuter Lungenembolie. Dies gilt auch für normotensive Patienten, bei denen eine akute Rechtsherzdysfunktion die Kurzzeitmortalität um das Zwei- bis Zehnfache erhöht.7 Ein vom Notarzt durchgeführtes bettseitiges Echokardiogramm kann die körperliche Untersuchung, das EKG und Biomarker ergänzen, um diese Patienten schnell zu identifizieren, Managemententscheidungen zu treffen und die endgültige Disposition festzulegen.
Tipps zur Beurteilung des rechten Herzens:
1. Sonde: Phased Array
2. Verwenden Sie die traditionellen 4 begrenzten Echokardiogramm-Ansichten: parasternale lange Achse (PSLA), parasternale kurze Achse (PSSA), apikale 4 Kammer (A4C), subxiphoid
3. Parasternale kurze Achse:
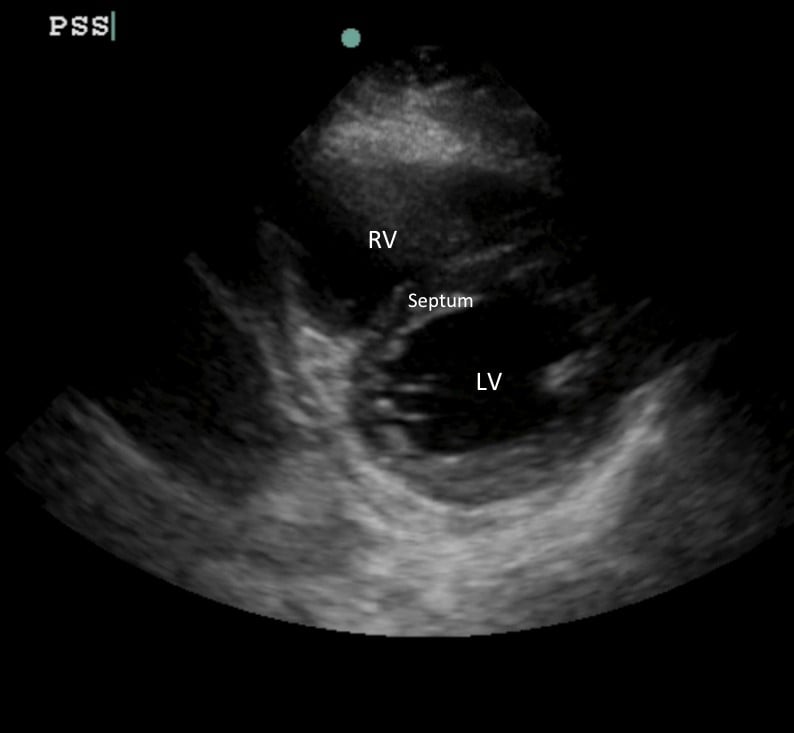
Bild 1: Normales halbmondförmiges RV und konzentrisches LV
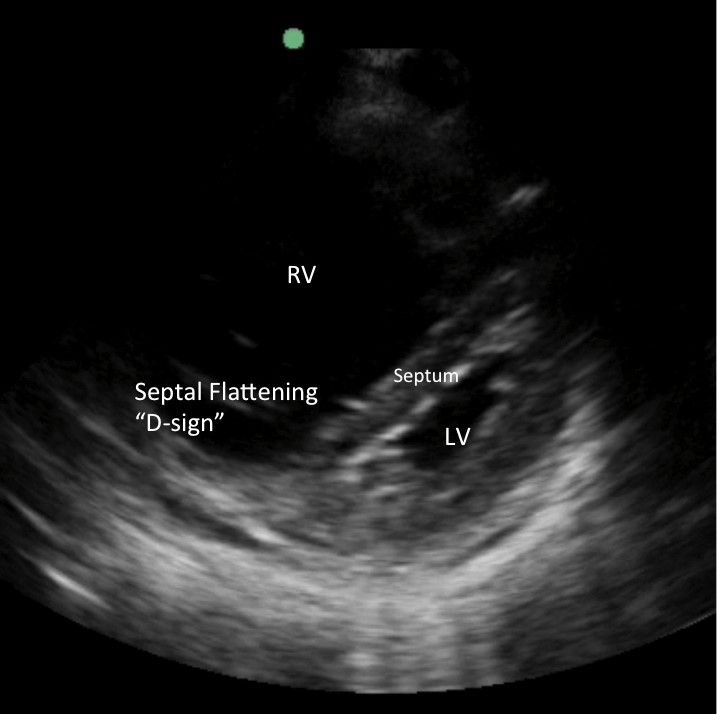
Bild 2: RHS mit abgerundetem, dilatiertem RV und Abflachung des Interventrikelseptums während der Diastole („D-Zeichen“ durch erhöhten RV-Druck)
4. Apikale 4 Kammer:
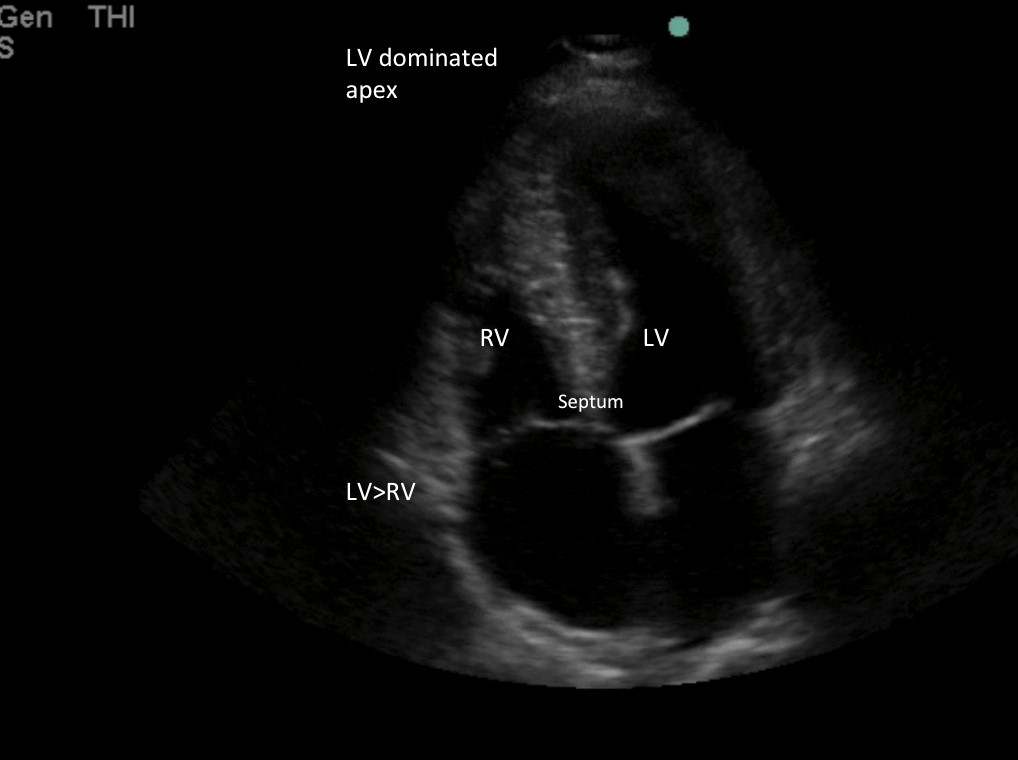
Bild 3: Normale RV-Größe weniger als ⅔ der LV-Größe und Apex dominiert durch LV
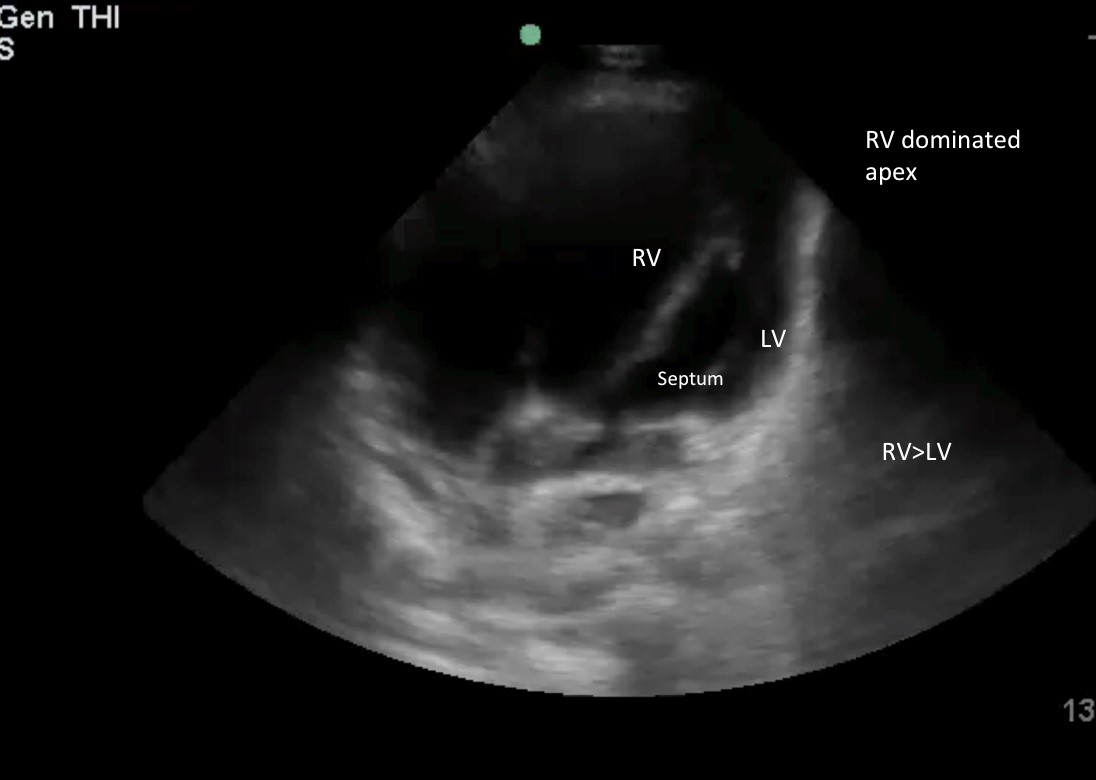
Bild 4: RV-Größe > ⅔ der LV-Größe und Apex dominiert von RV
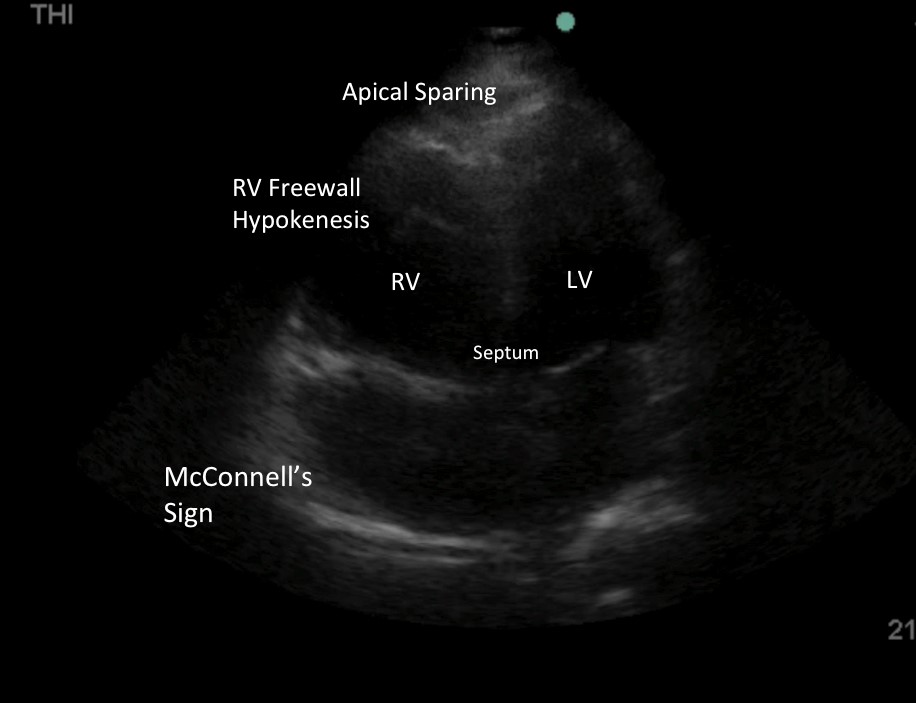
Bild 5: McConnell’s Sign: Hypokinese der freien RV-Wand mit erhaltenem apikalen Squeeze. Ursprüngliche Daten legten nahe, dass das McConnell-Zeichen ein spezifischer Indikator für eine akute PE ist, im Gegensatz zu der gleichmäßigeren Hypokinese, die bei chronischer primärer oder sekundärer pulmonaler Hypertonie (PHTN) zu erwarten ist. Neuere Daten widerlegen diese Schlussfolgerung, da das McConnell-Zeichen auch bei PHTN gesehen wird.8-9
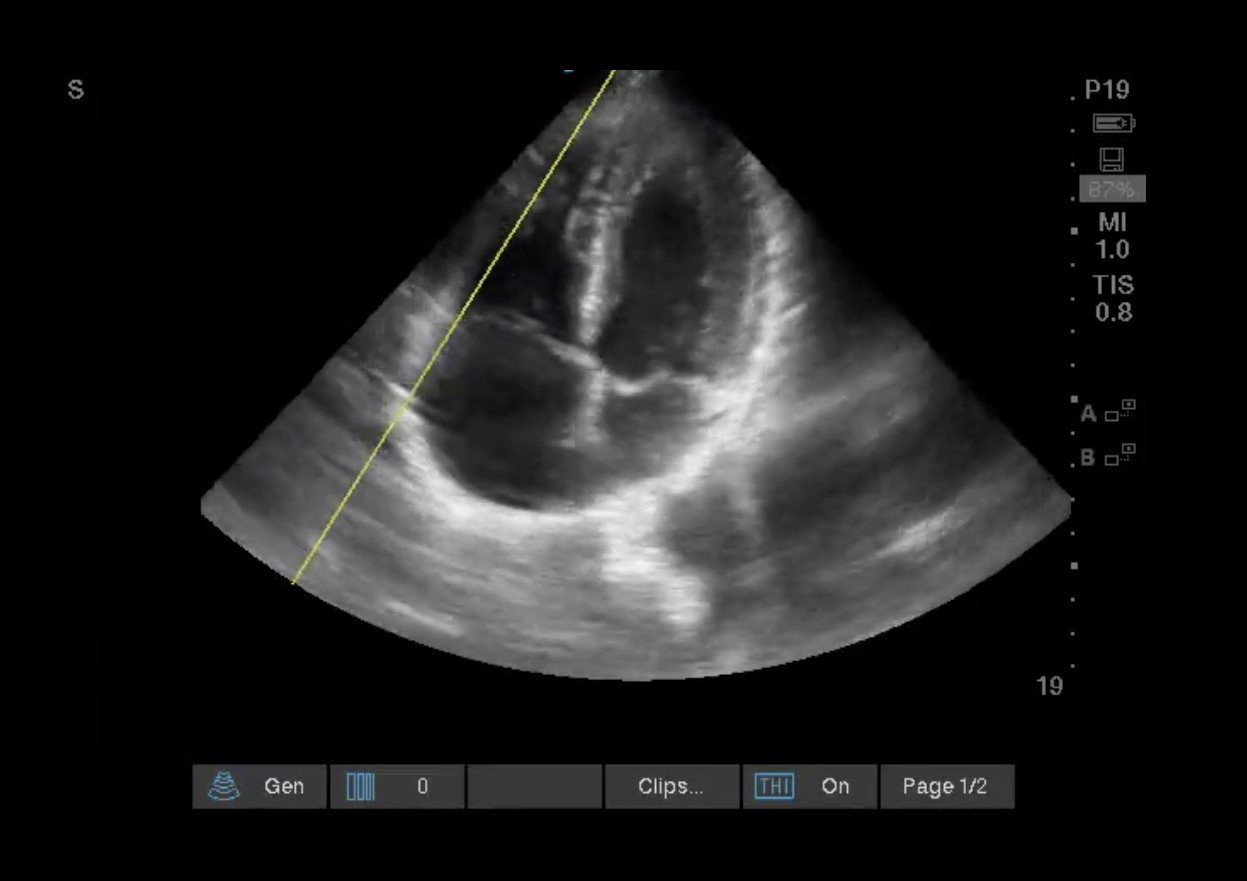
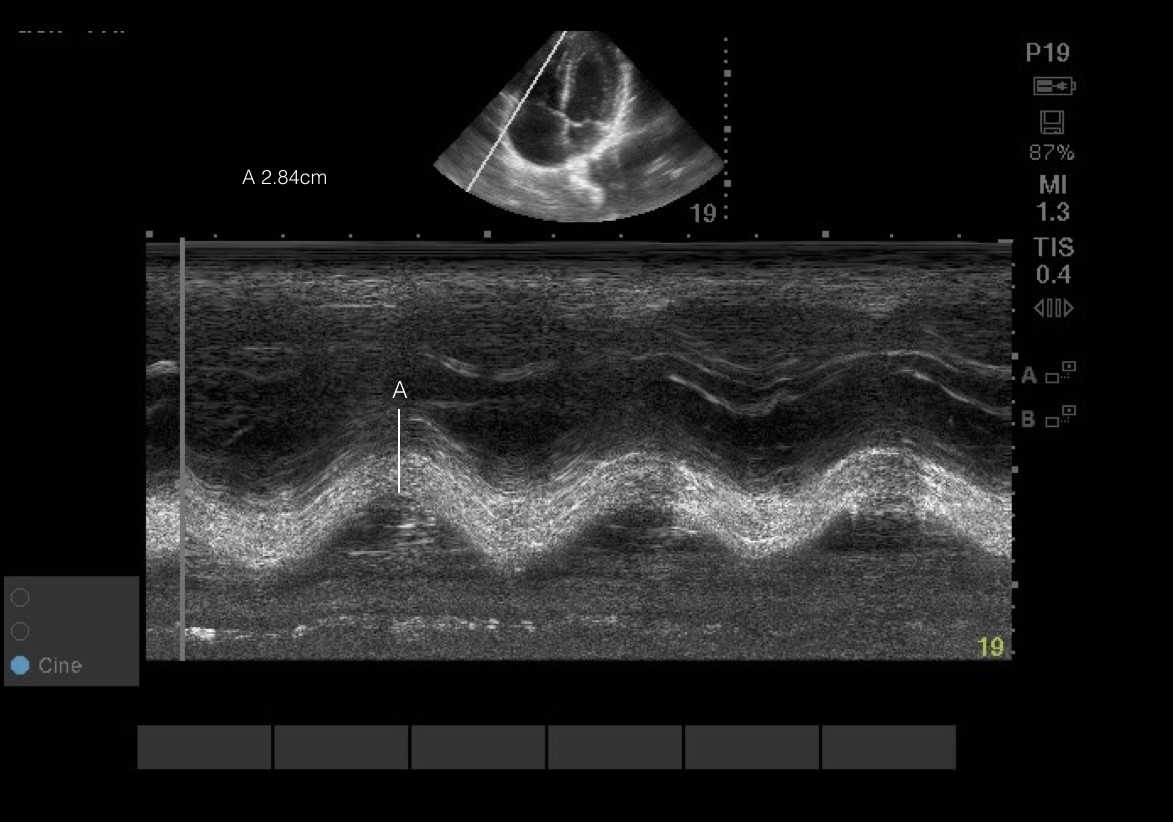
Bilder 6, 7 & Video 1 TAPSE: Das RV kontrahiert primär in der longitudinalen Ebene vom Apex zur Basis. Daher kann die Auswertung der seitlichen freien Bewegung auf die Sonde zu und von ihr weg (TAPSE) und die Stärke dieser Kontraktion (S‘) als Surrogatmarker für die systolische Funktion des RV dienen. Zur Durchführung platzieren Sie den M-Mode-Cursor durch die laterale freie Wand auf Höhe des Trikuspidalanulus, um eine Sinuswelle zu erhalten. Messen Sie von der Spitze bis zum Tal oder der maximalen systolischen und diastolischen Auslenkung. Abnormaler TAPSE<16mm. Für S‘: Platzieren Sie den Pulswellendoppler über der lateralen freien Wand knapp distal zum lateralen Anulus. Messen Sie die maximale Geschwindigkeit über der Basislinie. Abnormales S‘ < 9,5cm/s
Fallen: TAPSE und S‘ sind winkelabhängig. Daher verschlechtert sich ihre Fähigkeit zur Beurteilung der RV-Funktion bei A4C-Ansichten von schlechter Qualität erheblich. Darüber hinaus bewerten diese Surrogatmarker den RV nur in einer Ebene; Patienten können eine signifikante RV-Dysfunktion mit normalem TAPSE/S‘ haben. Trotz dieser Einschränkungen korrelieren TAPSE/S‘ mit der Morbidität der RV-Dysfunktion bei Patienten mit pulmonaler HTN.
5. Sub-xiphoid (keine Bilder)
Die Messung der lateralen freien Wand im Vordergrund kann einen Hinweis auf die Chronizität der Erkrankung geben. Normal <5mm, größer als 5mm deutet auf ein chronisches RHS hin.
Pitfall: Patienten mit chronischer Herzinsuffizienz können akut dekompensieren. Daher ist die Messung der freien Wand bei <5mm am besten als „rule out chronic RHS“ zu verwenden.
Schlussfolgerung
Gesamtheitlich betrachtet: Die Bewertung der rechtsventrikulären Dilatation, der abnormalen Septalbewegung, der Hypokinese der rechtsventrikulären freien Wand und der Surrogatmarker der systolischen Funktion des rechten Ventrikels ermöglicht dem Notarzt eine schnelle Beurteilung der Rechtsherzfunktion und die Einleitung einer lebensrettenden Therapie.
1. Ryan JJ, Tedford RJ. Diagnose und Behandlung des versagenden rechten Herzens. Curr Opin Cardiol. 2015;30(3):292-300.
2. Soni NJ, Arntfield R, Kory P. Point of Care Ultrasound E-book. Elsevier Health Sciences, 2014, 110-118.
3. Kossaify A. Echocardiographic assessment of the right ventricle, from the conventional approach to speckle tracking and three-dimensional imaging, and insights into the „Right Way“ to explore the forgotten chamber. Clin Med Insights Cardiol. 2015;9:65-75.
4. Silverstein MD, Heit JA, Mohr DN, et al. Trends in the incidence of deep vein thrombosis and pulmonary embolism: a 25-year population-based study. Arch Intern Med. 1998; 158: 585-93.
5. Horlander KT, Mannino DM, Leeper KV. Pulmonal embolism mortality in the United States, 1979-1998. An analysis using multiple-cause mortality data. Arch Intern Med. 2003;163(14):1711-1717. doi:10.1001/archinte.163.14.1711
6. Stein PD, Henry JW. Prävalenz der akuten Lungenembolie bei Patienten in einem Allgemeinkrankenhaus zum Zeitpunkt der Autopsie. Chest. 1995; 108: 978-81.
7. Matthews JC, McLaughlin V. Acute right ventricular failure in the setting of acute pulmonary embolism or chronic pulmonary hypertension: Ein detaillierter Überblick über die Pathophysiologie, Diagnose und Behandlung. Curr Cardiol Reviews. 2008, 4, 49-59.
8. Mediratta A, Addetia K, Medvedofsky D, et al. Echocardiographic diagnosis of acute pulmonary embolism in patients with McConnell’s Sign. Echocardiography. 2016;33(5):696-702. doi:10.1111/echo.13142.
9. Walsh BM, Moore CL. McConnell’s Sign ist nicht spezifisch für eine Lungenembolie: Fallbericht und Überblick über die Literatur. J Emerg Med. 2015;49(3):301-304.
10. Daley J, Grotberg J, Pare J, et al. Vom Notarzt durchgeführte systolische Exkursion der Trikuspidalebene bei der Bewertung einer vermuteten Lungenembolie. Am J Emerg Med. 2017;35:106-111.
Zurück zum Newsletter