¿Te has preguntado alguna vez «cuál es la diferencia entre el pH y la alcalinidad? Muchos de nosotros en la acuariofilia confundimos la alcalinidad total y el pH. Es comprensible, dado lo borrosa que es la línea entre palabras como «alcalino» y «alcalinidad». Efectivamente, la alcalinidad y el pH en la química del agua están muy relacionados, pero no son lo mismo. Este artículo distinguirá entre ellos.
Escucha este tema en nuestro Podcast:
¿Qué es el pH?
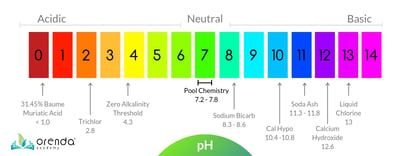 La escala de pH
La escala de pHEl pH son las siglas de Hidrógeno potenz, más comúnmente conocido como «poder del Hidrógeno». Es el logaritmo negativo de la concentración de iones de hidrógeno en una solución. Cuanto más bajo sea el pH, mayor será la cantidad de hidrógeno.
PH = -log(H+)
Medimos lo ácidas o básicas (también llamadas alcalinas) que son las sustancias utilizando la escala de pH. La escala de pH va de 0 a 14, y es relativa al agua pura, que tiene un pH perfectamente neutro de 7. Cuando la concentración de iones de hidrógeno sube, el pH baja (y viceversa). La escala es logarítmica, lo que significa que cada número entero de la escala de pH del 1 al 14 es 10 veces mayor o menor que los números que lo rodean. Por ejemplo, algo con un pH de 6,0 sería 10 veces más ácido que el agua destilada con un pH de 7,0. Algo con un pH de 5,0 es 10 veces más ácido que 6,0, y 100 veces más ácido que 7,0 (10×10=100).
Para poner la escala de pH en perspectiva, hagamos algunos cálculos rápidos. El tricloro, un tipo popular de cloro estabilizado que se utiliza principalmente en las piscinas al aire libre, tiene un pH de alrededor de 3. Para este cálculo, vamos a redondear exactamente a 3,0. ¿Cómo de ácido es el Tricloro de 3.0pH comparado con el agua de 7.0pH? Averigüémoslo.
(7.0pH – 3.0pH) = 4.0
La escala logarítmica significa 104, o 10x10x10x10 = 10.000
El tricloro es unas 10.000 veces más ácido que el agua pura.
No te preocupes por las matemáticas, es sólo para explicar la escala de pH en sí. Desde el punto de vista de la química del agua, los libros de texto nos dicen que el pH ideal para una piscina o spa está entre 7,4-7,6. Pero siendo realistas, el pH aumenta con el tiempo en la mayoría de las piscinas, por lo que el rango normal de una piscina es más bien de 7,4 a 8,2.
Las funciones del pH en la química del agua
Fuerza del cloro (%HOCl)
La gestión del pH es un componente crítico para mantener una química del agua saludable y equilibrada. Es tan importante porque el pH es un factor impulsor del Índice de Saturación de Langelier (LSI), y también porque el pH determina la eficacia del cloro en piscinas no estabilizadas. Así, en piscinas sin ácido cianúrico (CYA), cuanto más bajo sea el pH, más fuerte será el cloro, porque el pH controla los equilibrios de disociación entre el cloro fuerte y el débil:
HOCl ⇌ H+ + OCl-
El Ácido Hipocloroso se disocia en Hidrógeno e Ion Hipoclorito
De nuevo, el pH controla la fuerza del cloro (%HOCl) porque cuanto más bajo sea el pH, mayor será la concentración de Hidrógeno. Eso significa un mayor % de HOCl fuerte frente a OCl débil. Esto no es tan relevante en piscinas con CYA, porque los isocianuratos cambian fundamentalmente la química de la piscina.
 Solubilidad del carbonato de calcio
Solubilidad del carbonato de calcio
Mientras que el LSI determina cuando el agua está sobresaturada de carbonato de calcio (CaCO3), el pH es un factor importante en el LSI. Y como las violaciones del LSI se producen de forma local, no universal en toda la piscina, el pH importa mucho. Por ejemplo, hay un gráfico que muestra los equilibrios de los tipos de alcalinidad. Cuando el pH llega a 8,2 u 8,3, es muy difícil que el calcio permanezca en solución, porque la alcalinidad de carbonatos (CO3-) se une muy bien al calcio (Ca++). Por lo tanto, cuando el pH es demasiado alto, el calcio tiende a precipitarse fuera de la solución, incluso si el LSI general de la piscina está equilibrado. Vemos que este fenómeno enturbia las piscinas, como cuando alguien añade carbonato de sodio demasiado rápido.
El CO2 determina el pH
La cantidad de dióxido de carbono (CO2) en su agua determina en gran medida el pH. Cuanto más CO2, más bajo es el pH, y viceversa. Esto explica por qué las instalaciones acuáticas, los bordes de fuga y los chorros del spa aumentan el pH más rápidamente que en el agua tranquila; la aireación acelera la pérdida de CO2 a la atmósfera.
Consecuencias del pH
Un pH bajo disminuye el LSI, y puede causar daños en las superficies y el equipo, corrosión de los componentes metálicos de la piscina y sus alrededores, irritación de la piel y los ojos, así como malestar general del patrón. Por otro lado, un pH alto aumenta el LSI y provoca la formación de incrustaciones de carbonato, agua turbia y un cloro más débil (en piscinas no estabilizadas). Los libros de texto dicen que hay que mantenerse dentro del rango de 7,4-7,6 para evitar esos problemas, pero una estrategia basada en el LSI evitará los problemas mejor que simplemente permanecer en ese rango.
¿Qué es la alcalinidad total?
La alcalinidad total es una medida de la concentración de todas las sustancias alcalinas disueltas en el agua que pueden atraer y liberar iones de hidrógeno. Esta interferencia con el hidrógeno es la razón por la que la alcalinidad amortigua los cambios de pH. La alcalinidad total se compone principalmente de bicarbonato, carbonato e hidróxido, junto con algunos otros como la alcalinidad de cianurato. Cuando se añade ácido, estos álcalis tienen la capacidad de neutralizar parte del ácido. En términos más sencillos, la alcalinidad total es una medida de la capacidad del agua para resistir el cambio de pH. En concreto, la alcalinidad frena la reducción del pH. Un exceso de alcalinidad es en realidad una fuente de aumento del pH. Cuanta más alcalinidad tenga, más ácido se necesita para reducir el pH.
Relacionado: ¿Qué es la alcalinidad?
 La alcalinidad total se mide por su concentración en partes por millón (ppm), y el rango ideal es de 80-120 ppm, dependiendo del tipo de cloro que utilice. Por ejemplo, el tricloro tiene un pH bajo de 2,8, por lo que, dado lo ácido que es el tricloro, una piscina de tricloro necesita una mayor alcalinidad. Otra razón para una mayor alcalinidad en una piscina de tricloro es porque el CYA en el tricloro compensa la alcalinidad cuando se hacen correcciones de LSI.
La alcalinidad total se mide por su concentración en partes por millón (ppm), y el rango ideal es de 80-120 ppm, dependiendo del tipo de cloro que utilice. Por ejemplo, el tricloro tiene un pH bajo de 2,8, por lo que, dado lo ácido que es el tricloro, una piscina de tricloro necesita una mayor alcalinidad. Otra razón para una mayor alcalinidad en una piscina de tricloro es porque el CYA en el tricloro compensa la alcalinidad cuando se hacen correcciones de LSI.
Los cloros no estabilizados, como el cloro líquido (lejía) o el cal hypo, tienen cada uno un pH alto. Así que puede tener una alcalinidad más baja, como 80-100 ppm, o incluso más baja que 80 ppm si su LSI lo permite. Las piscinas de cloro salino suelen tener problemas con la acumulación de cal que se desprende de la célula de sal y entra en la piscina. Las piscinas de sal, en temporada, suelen beneficiarse de niveles más bajos de alcalinidad, como 60-70 ppm, siempre que el LSI se mantenga equilibrado. La clave es medir el ácido y diluirlo antes de verterlo para evitar correcciones excesivas. Demasiado ácido con una alcalinidad más baja causará problemas mayores, así que tenga cuidado.
¿Se ha dado cuenta de que la alcalinidad total no se mide en la escala de pH?
Es una distinción importante que hay que hacer, porque así es como se suelen confundir el pH y la alcalinidad. La alcalinidad total se mide por la cantidad o concentración (ppm) en el agua, no por el grado de alcalinidad (pH) del agua. Los productos para aumentar la alcalinidad son frecuentes en el sector de las piscinas. Si busca un producto para aumentar la alcalinidad, los dos más comunes son el bicarbonato de sodio (NaHCO3) y el carbonato de sodio (Na2CO3), más conocido como ceniza de sosa. Los productos «bajadores de la alcalinidad» serán un ácido como el ácido muriático o el bisulfato de sodio.
El papel de la alcalinidad total en la química del agua
Si usted es un operador de piscinas, probablemente ya sabe que el pH puede fluctuar hacia arriba y hacia abajo. Y cuando lo hace, la piscina está constantemente luchando en su contra. Tener el nivel correcto de alcalinidad total es algo bueno, porque ayuda a mantener el pH estabilizado. Una forma sencilla de pensar en la alcalinidad es que aísla el pH para que no cambie con demasiada facilidad, especialmente cuando baja.
Técnicamente, la alcalinidad amortigua el pH liberando o absorbiendo un ion hidrógeno (H+) según sea necesario. Así que cuando se añade ácido, los iones de carbonato pueden absorber hidrógeno para crear iones de bicarbonato. Esto es un equilibrio, al igual que el pH, por lo que también puede ir en sentido contrario. El equilibrio se ve así:
HCO3- + H+ ↔ H2CO3
Como el CO2 controla el pH del agua, puedes añadir CO2 directamente para bajar el pH, o puedes usar ácido para convertir la alcalinidad del bicarbonato en ácido carbónico (H2CO3), que es sólo CO2 disuelto: (H2O + CO2 → H2CO3).

Podría añadir varios kilos de bicarbonato de sodio de 8,3pH y conseguir el mismo impacto en el pH si añadiera una cantidad mucho menor de ceniza de sosa de 11,6 pH. Pero la alcalinidad total sería más alta para el Bicarbonato de Sodio, porque simplemente hay más de él en el agua.
Cómo aumentar la alcalinidad total y el pH
Si quiere aumentar la alcalinidad total en una piscina, necesita saber el galonaje de la piscina, y su pH. Es útil tener una calculadora de dosificación precisa. Aumentar la alcalinidad es tan sencillo como añadir bicarbonato sódico al agua.
Relacionado: Cómo subir la alcalinidad y el pH
Cómo bajar la alcalinidad total y el pH
Puedes bajar la alcalinidad usando ácido. Algunos expertos recomiendan un «vertido de columna de ácido» para bajar la alcalinidad, pero nosotros no lo hacemos. Según nuestra experiencia -y de hecho, los experimentos científicos lo respaldan- el vertido en columna es más perjudicial que la dilución. Recomendamos diluir el ácido en un cubo de agua y verterlo uniformemente por la piscina. Además, el vertido en columna puede reducir mucho el pH en un lugar concentrado (en el fondo de la piscina), lo que puede desviar el LSI y, a su vez, grabar la superficie. Bajar el pH sin afectar a la alcalinidad total puede conseguirse inyectando dióxido de carbono. Pero ese es un tema para otra ocasión.
Relacionado: Cómo bajar el pH y la alcalinidad
Conclusión
Mantenga su piscina dentro del equilibrio LSI, en primer lugar. Luego, trate de mantener su alcalinidad en un rango que sea más ventajoso para su tipo de cloro primario. Utilice un incrementador de la alcalinidad, como el bicarbonato sódico, para aumentar la alcalinidad total, o un ácido para reducirla. Si utiliza cloros de alto pH, como los generadores de cloro salino, el cloro líquido o el hipoclorito de calcio, necesitará menos alcalinidad, como 60-80 ppm. Para los cloros de bajo pH, como el tricloro, 100-120 ppm puede ser un rango mejor para ti. Consulta tu kit de pruebas o la calculadora de dosificación en la App de Orenda para conocer los números específicos.
Como apunte, nunca mezcles diferentes tipos de cloro. Pueden explotar. Literalmente.
La gente confunde el pH con la alcalinidad y podemos entender por qué. Sólo hay que recordar que el pH es un equilibrio que nos dice lo ácida o básica que es una solución. La alcalinidad total mide la cantidad o concentración (en partes por millón) de álcali disuelto que puede amortiguar el cambio de pH liberando o atrayendo hidrógeno. Esperamos que esto ayude!